Son yıllarda yaşlanma ve yaşlılığa bağlı hastalıklar ile ilgili araştırmalara yapılan yatırım ciddi bir artış gösterdi ve herkes gençlik formülünü gizliden gizliye beklemekte. Açılan gerontoloji bölümleri, yüksek lisans alanları ve Türkiye'nin de yaşlanmakta olan bir nüfusa sahip olduğu göz önüne alınarak açılan yaşlı bakım evleri, üniteleri , kurum ve kuruluşları var. Yaşlanmanın bilinen en temel sebebi telomerlerin kısalarak DNA bölünmelerine izin vermemesi, ve hasta olan hücrelerin bölünememe sebebiyle yenilenememesi ve yaşlanarak ölmesidir. Hatta yaşlılığa bağlı olan rahatsızlıkların, hastalıkların ve hatta ölümün de temel sebebi telomerlerin kısalmasıdır.
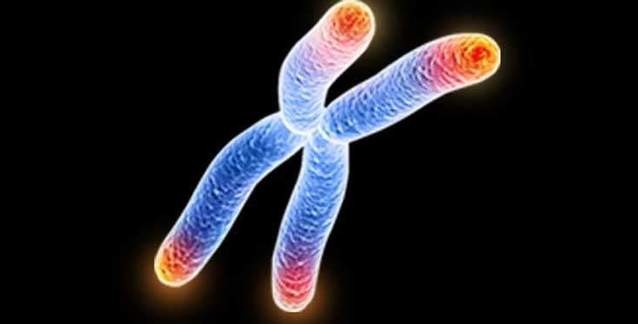
Peki telomer nedir? Telomerler kromozom denilen DNA zincirlerinin uçlarındaki anlamsız nükleotit dizileridir ve asıl anlamlı olan genleri koruyucu bir işlevi vardır. Genç insanlarda 8.000 ila 10000 nükleotitten oluşan telomerler, her hücre bölünmesinde uç kısımdan bir miktar nükleotit kaybederek kısalır. Öyle ki, belli bir eşik değerine geldiğinde hücre bölünemez hale gelir ve ölür. Hatta bu sebeptendir ki, laboratuvar araştırmaları sırasında hücreler bir kaç bölünmeden sonra çok fazla telomer nükleotiti kaybederek ölür ve araştırmayı zora sokar.Toplum içinde 'ecel' olarak bilinen bu duruma biyolojik olarak bir 'iç saat' - telomer uzunluğu - karar veriyor.
Son zamanlarda Stanford Üniversitesi Tıp Fakültesi araştırmacıları tarafından yapılan bir araştırma ile, insan telomerleri laboratuvar ortamında hızlı ve etkili bir şekilde uzatıldı. Telomerleri uzatılan insan deri hücreleri, diğerlerine göre çok daha genç gibi davrandılar ve ölmek şöyle dursun, 40'dan fazla kez bölünmeye devam ettiler.
Burada uygulanan prosedürde de kullanılan, birçok ilaçta kullanılan etken maddeyle aynı, ' modifiye RNA '.
Bu araştırma ile hücrelerin ömrü uzatılıyor ve bu her şeyden önce ilaç testlerin daha sağlıklı ve uzun süre yapılabileceğini, hastalık modellemelerinin daha kolaylıkla yapılabileceğini gösteriyor. Bulunan yöntem ile telomer uzunluğu 1000 nükleotit kadar uzatıldı ve böylece insan yılıyla bir kaç yıl fazla ömüre tekabül ediyor. Araştırma 26 Ocak 2015 tarihinde FASEB Journal 'de yayımlandı.
Prosedürde mRNA (messenger -mesajcı- RNA)'nın modifiye bir versiyonu kullanıldı.Bu mRNA hangi proteinin kodunu taşıyor? derseniz, ' telomeraz 'denen, kök hücreler tarafından sentezlenen, telomer uzamasında görev alan, kök hücrelerde çıkça bulunan ve de doğal olarak hücrede bulunan bir enzimin aktif (görev yapan ya da substrata bağlanan) kısmı olan TERT bileşeninin kodunu taşıyor. Burada moleküler biyolojinin cilveleriyle karşı karşıyayız. TERT, telomerleri uzatan, sonlarına TTAGGG nükleotit dizilimlerini ekleyen, ve bölünme sayısını artıran bir görev yapıyor. Ama telomerlerin sürekli uzaması iyi bir anlam ifade etmez çünkü sürekli bölünme kanserli hücre oluşumuna sebebiyet verir. Bizim modifiye mRNA'mız ise çok avantaj sağlıyor çünkü TERT'in hücre içinde biraz daha uzun süre kalıp görev yapmasını sağladıktan sonra (yaklaşık 48 saat) yok oluyor ve uzatılmış telomerler yeniden sağlıklı bir şekilde hücre bölündükçe kısalmaya devam ediyor.
Bir kaç gün içinde üst üste 3 ayrı uygulamada insan kas ve deri hücrelerinde sağlıklı bir şekilde telomer uzamasını sağladılar:
Modifiye RNA 'yı bir kaç gün içinde bir çalışma için çok küçük bir sayı olan üç uygulamada deneyerek insan kas ve deri hücrelerinde sağlıklı bir şekilde telomer uzatılması başarıldı. 1.000 nükleotit eklenmesiyle yaklaşık %10`luk bir uzama kaydedildi, ve söz konusu hücrelerde, normal telomere sahip hücrelere oranla ortalama 40 bölünme fazladan kaydedildi.
Bu yeni yaklaşım, yaşlılığa bağlı hastalıkların önlenmesi ve tedavisinde yeni bir yol açmakta. Aynı zamanda, telomer kısalması ile ilişkilendirilen, hastayı elden ayaktan düşüren genetik hastalıklar için de bu potansiyel tedaviden yararlanılabilecek.
Önceki çalışmalar ise Duchenne muskuler distrofi hastası erkeklerin kas kök hücrelerinin sağlıklı erkeklerden çok daha kısa telomere sahip olduğunu gösterdi. Bu sonuç, hücrelerin yeni kaslar yapmak için nasıl çalıştığı ya da çalışmadığını anlayabilmemizi sağlamasının yanı sıra, hasarlı hücrelerin laboratuvar ortamındaki sınırlı büyüme yeteneğinin de açıklanabilmesine yardımcı oldu.
Araştırmacılar tekniklerinin ve yöntemin diğer hücre çeşitlerinde de çalışıp çalışmayacağını deniyorlar. Bu metodun ve uygulama alanlarının genişletilmesi için araştırmalar başladı bile. Hedefler ise hiç de hayal değil, örneğin Duchenne muskuler (kas) distrofi hastalığını iyileştirmek için, hastalardaki kök hücreler hedeflenerek telomerleri uzatılabilir, yaşlanmaya bağlı şeker ve kalp hastalıkları iyileştirilebilir ve kısacası gençleşilebilir.
Referans :
J. Ramunas, E. Yakubov, J. J. Brady, S. Y. Corbel, C. Holbrook, M. Brandt, J. Stein, J. G. Santiago, J. P. Cooke, H. M. Blau. Transient delivery of modified mRNA encoding TERT rapidly extends telomeres in human cells. The FASEB Journal, 2015; DOI: 10.1096/fj.14-259531
Peki telomer nedir? Telomerler kromozom denilen DNA zincirlerinin uçlarındaki anlamsız nükleotit dizileridir ve asıl anlamlı olan genleri koruyucu bir işlevi vardır. Genç insanlarda 8.000 ila 10000 nükleotitten oluşan telomerler, her hücre bölünmesinde uç kısımdan bir miktar nükleotit kaybederek kısalır. Öyle ki, belli bir eşik değerine geldiğinde hücre bölünemez hale gelir ve ölür. Hatta bu sebeptendir ki, laboratuvar araştırmaları sırasında hücreler bir kaç bölünmeden sonra çok fazla telomer nükleotiti kaybederek ölür ve araştırmayı zora sokar.Toplum içinde 'ecel' olarak bilinen bu duruma biyolojik olarak bir 'iç saat' - telomer uzunluğu - karar veriyor.
Son zamanlarda Stanford Üniversitesi Tıp Fakültesi araştırmacıları tarafından yapılan bir araştırma ile, insan telomerleri laboratuvar ortamında hızlı ve etkili bir şekilde uzatıldı. Telomerleri uzatılan insan deri hücreleri, diğerlerine göre çok daha genç gibi davrandılar ve ölmek şöyle dursun, 40'dan fazla kez bölünmeye devam ettiler.
Burada uygulanan prosedürde de kullanılan, birçok ilaçta kullanılan etken maddeyle aynı, ' modifiye RNA '.
Bu araştırma ile hücrelerin ömrü uzatılıyor ve bu her şeyden önce ilaç testlerin daha sağlıklı ve uzun süre yapılabileceğini, hastalık modellemelerinin daha kolaylıkla yapılabileceğini gösteriyor. Bulunan yöntem ile telomer uzunluğu 1000 nükleotit kadar uzatıldı ve böylece insan yılıyla bir kaç yıl fazla ömüre tekabül ediyor. Araştırma 26 Ocak 2015 tarihinde FASEB Journal 'de yayımlandı.
Prosedürde mRNA (messenger -mesajcı- RNA)'nın modifiye bir versiyonu kullanıldı.Bu mRNA hangi proteinin kodunu taşıyor? derseniz, ' telomeraz 'denen, kök hücreler tarafından sentezlenen, telomer uzamasında görev alan, kök hücrelerde çıkça bulunan ve de doğal olarak hücrede bulunan bir enzimin aktif (görev yapan ya da substrata bağlanan) kısmı olan TERT bileşeninin kodunu taşıyor. Burada moleküler biyolojinin cilveleriyle karşı karşıyayız. TERT, telomerleri uzatan, sonlarına TTAGGG nükleotit dizilimlerini ekleyen, ve bölünme sayısını artıran bir görev yapıyor. Ama telomerlerin sürekli uzaması iyi bir anlam ifade etmez çünkü sürekli bölünme kanserli hücre oluşumuna sebebiyet verir. Bizim modifiye mRNA'mız ise çok avantaj sağlıyor çünkü TERT'in hücre içinde biraz daha uzun süre kalıp görev yapmasını sağladıktan sonra (yaklaşık 48 saat) yok oluyor ve uzatılmış telomerler yeniden sağlıklı bir şekilde hücre bölündükçe kısalmaya devam ediyor.
Bir kaç gün içinde üst üste 3 ayrı uygulamada insan kas ve deri hücrelerinde sağlıklı bir şekilde telomer uzamasını sağladılar:
Modifiye RNA 'yı bir kaç gün içinde bir çalışma için çok küçük bir sayı olan üç uygulamada deneyerek insan kas ve deri hücrelerinde sağlıklı bir şekilde telomer uzatılması başarıldı. 1.000 nükleotit eklenmesiyle yaklaşık %10`luk bir uzama kaydedildi, ve söz konusu hücrelerde, normal telomere sahip hücrelere oranla ortalama 40 bölünme fazladan kaydedildi.
Tedavi için Potansiyel Kullanım Alanları
Bu yeni yaklaşım, yaşlılığa bağlı hastalıkların önlenmesi ve tedavisinde yeni bir yol açmakta. Aynı zamanda, telomer kısalması ile ilişkilendirilen, hastayı elden ayaktan düşüren genetik hastalıklar için de bu potansiyel tedaviden yararlanılabilecek.
Önceki çalışmalar ise Duchenne muskuler distrofi hastası erkeklerin kas kök hücrelerinin sağlıklı erkeklerden çok daha kısa telomere sahip olduğunu gösterdi. Bu sonuç, hücrelerin yeni kaslar yapmak için nasıl çalıştığı ya da çalışmadığını anlayabilmemizi sağlamasının yanı sıra, hasarlı hücrelerin laboratuvar ortamındaki sınırlı büyüme yeteneğinin de açıklanabilmesine yardımcı oldu.
Araştırmacılar tekniklerinin ve yöntemin diğer hücre çeşitlerinde de çalışıp çalışmayacağını deniyorlar. Bu metodun ve uygulama alanlarının genişletilmesi için araştırmalar başladı bile. Hedefler ise hiç de hayal değil, örneğin Duchenne muskuler (kas) distrofi hastalığını iyileştirmek için, hastalardaki kök hücreler hedeflenerek telomerleri uzatılabilir, yaşlanmaya bağlı şeker ve kalp hastalıkları iyileştirilebilir ve kısacası gençleşilebilir.
Atardamar duvarı hücrelerindeki telomerler, toplardamar duvarındakilerinkilerden genellikle daha kısadır. Bu farklılık, stres ve gerilim altındaki atardamarların güç yaşantısını yansıtır çünkü atardamarlardaki kan, yüksek basınca maruz kalır. Atardamarlar, her nabız atımında genişleyip büzülerek, daha fazla hasara uğrar ve onarıma ihtiyaç duyar. onarım, telomer uçlarının harcandığı hücre kopyalamasıyla yapılır. Böylece hücreler yaşlanmaya başlar ve biz, toplardamarların değil atardamarların sertleşmesi yüzünden hayatımızı kaybederiz.
– Matt Ridley (Genom – ISBN: 9786054238811)
Referans :
J. Ramunas, E. Yakubov, J. J. Brady, S. Y. Corbel, C. Holbrook, M. Brandt, J. Stein, J. G. Santiago, J. P. Cooke, H. M. Blau. Transient delivery of modified mRNA encoding TERT rapidly extends telomeres in human cells. The FASEB Journal, 2015; DOI: 10.1096/fj.14-259531
Bu içerik BilimFili.com yazarı tarafından oluşturulmuştur. BilimFili.com`un belirtmiş olduğu "Kullanım İzinleri"ne bağlı kalmak kaydıyla kullanabilirsiniz.
Kaynak ve İleri Okuma
Etiket
Projelerimizde bize destek olmak ister misiniz?
Dilediğiniz miktarda aylık veya tek seferlik bağış yapabilirsiniz.
Destek Ol
Yorum Yap (0)
Bunlar da İlginizi Çekebilir

07 Temmuz 2016
Yaşlanmayı Kaçınılmaz Kılan Biyoloji Değil Fizik

31 Ocak 2017
Telomer Nedir?

22 Şubat 2016
Yaşlanma ve Genetik İlişkisinde Yeni Keşif

25 Haziran 2017
İleri Yaşta Cinsel Aktivite Beyin Gücüne Katkı Yapabiliyor