Canlılığın her aşamasında birincil görevler üstlenen proteinlerin, belirli bir sırada arka arkaya birbirlerine eklenen amino asitlerden oluşan zincirler olduğunu biliyoruz. Ancak bir proteinin kimliğini belirlemede, onu oluşturan amino asitlerin dizilim sırası kadar önemli bir özelliği daha bulunur: Proteinin üç boyutlu yapısının katlanma biçimi.
Proteinlerin yapı taşları ve katlanışları, onların işlevlerini belirler. Organizmanın yaşamsal süreçlerinin yürütülmesinde görev alan her proteinin amino asit dizilimi de, üç boyutlu katlanma biçimi de bellidir. Eğer dizilişte ya da katlanışta bozulma olursa, protein görevini yerine getiremez; hatta bu durum bazen organizma sağlığını tehlikeye atacak sonuçlar doğurur. Çünkü "prion" adı verilen yanlış katlanmış proteinler, edindikleri hatalı biçimi düzgün proteinlere de bulaştırabilir. Bu yolla oluşan prion hastalıklarına örnek olarak sığırlardaki Deli Dana Hastalığı, koyunlardaki Sıyırtma (İng. Scrapie) Hastalığı, geyiklerdeki Kronik Tükeniş Hastalığı (İng. chronic wasting disease), insanlardaki Kuru Hastalığı, Creutzfeldt–Jakob Hastalığı ve Gerstmann–Sträussler–Scheinker Sendromu örnek verilebilir.
2006 yılında Brezilya'da çalışan araştırmacılar tarafından, prionların yaşamın ortaya çıkış öyküsünde oynamış olabilecekleri role ilişkin bir makale Medical Hypotheses dergisinde yayımlandı. Bu makalenin Türkçe çevirisini sunuyoruz.
Özet
DNA ve RNA, genetik bilginin depolanması ve işlenmesi ile ilgili modern hücresel moleküllerdir. Ancak, Dünya'nın eskiden sahip olduğu ortam koşullarında, çok karmaşık olmalarından ve ısıya duyarlılıklarından ötürü, iki molekül de bu işlevler için en iyi seçenek olmaktan çok uzaktır. Yapılan deneyler, proteinlerin çok uç koşullarda bile çok kararlı ve güvenilir moleküller olduklarını ve belirli koşullar altında, Mendelyen olmayan bir şekilde kalıtılan bazı fenotiplerin aktarımıyla ilişkili olabileceklerini gösteriyor.
Prionlar, yanlış katlanmış bir protein tarafından proteinlerin katlanışlarının değiştirilmesi sonucu memelilerde görülen bazı nörolojik hastalıklarla ilişkilendirilen bulaşıcı proteinlerdir ve en uç ortamlara karşı bile çok dirençlilerdir. Dahası, epigenetik bir modelde, prionlar bazı mantargil özelliklerinin aktarımıyla da ilişkilendirilir. Bu iki özellik, prionların erken dönem peptit evriminin bir kalıntısı olabileceği ve bilginin biyolojik aktarımının, modern nükleik asitlerle temsil edilen dijital (sayısal) kodundan farklı olarak, çok eski zamanlardan kalma bir analog (örneksel) kodunun kalıntısını temsil edebileceği hipotezini destekler.
Giriş
Dünya üzerindeki canlılığın, gezegen tarihinin başlarında doğduğu, günümüzde genel kabul görmektedir. Ancak, canlılığın belirmesiyle ilgili mekanizmalar hâlâ çok tartışmalıdır. Gezegenimizdeki yaşamın en başında, modern DNA örüntüsünün bir genetik bilgi deposu görevi görmesi, kimyasal açıdan gerçekçi değildir. DNA, proteinlerin sentezlenmesi için gereken genetik bilgiyi taşır. DNA'nın eşlenmesi ve yazımı ise enzimlerden ve başka proteinlerden oluşan karmaşık bir kümeyi gerektirir. En kısa DNA ipliğinin bile eşlenmesine yardım edecek proteinlere gereksinimi olur. O hâlde DNA-bazlı moleküler biyolojiye sahip ilk canlı hücreler, canlılık-öncesi (pre-biyotik) Dünya üzerindeki spontane kimyasal süreçlerle nasıl başlayabilir? İlk başlardaki DNA sentezi, spesifik enzimlerin varlığını gerektirmiş olmalıdır ama DNA'daki genetik bilgi olmadan ve RNA o bilgiyi protein enzimlerin amino asit dizisine çevirmeden, bu enzimler nasıl sentezlenmiş olabilir? Bir başka deyişle, DNA sentezi için proteinler gerekir; protein sentezi için de DNA gerekir. Bundan başka, DNA'nın büyük kimyasal karmaşıklığı ve ısıya duyarlılığı, DNA'yı kendini eşleme ve genetik bilginin güvenilir biçimde aktarımı mekanizmalarının, muhtemelen sonradan geliştirilmiş bir şekli yapar.
RNA Dünyası
Çoğu bilimci, ilk başlardaki yaşamla ilgili olmak için RNA'yı çok daha uygun bir molekül olarak görür. "RNA Dünyası" terimi ilk olarak Walter Gilbert tarafından 1986'da kullanılmıştır. RNA Dünyası hipotezi, RNA'nın tıpkı DNA gibi genetik bilgiyi depolama, aktarma ve iki katına çıkarma yetisiyle desteklenmiştir. RNA ayrıca ribonükleik asitten oluşan bir enzim olan ribozim görevi de görebilir. Hem DNA'nın hem de proteinlerin (enzimlerin) görevlerini gerçekleştirerek kendi kendine çoğalabildiği için RNA'nın bir zamanlar bağımsız yaşama sahip olmaya muktedir olduğu düşünülmüştür ve bazı RNA-virüsler bu yetinin yan etkilerini temsil ediyor olabilir. Viral RNA Q-beta gibi basit ribozimlerle yapılan deneyler, basit kendini-eşleyen RNA yapıların en güçlü seçilim baskılarına bile dayanabildiğini göstermiştir.
RNA'lar arası rekabet, farklı RNA zincirleri arası işbirliğinin belirmesini kayırarak, ilk proto-hücrenin oluşumuna kapı aralayabilir. Sonunda, amino asitlerin birbirlerine bağlanmasına (peptit bağlarına) yardım eden katalitik özellikli RNA zincirleri rastgele gelişmiştir. Bu amino asitler daha sonra RNA sentezine yardım ederek, ribozimler olarak görev yapan o RNA zincirlerine seçimsel avantaj vermiştir. Bu hipoteze göre, en sonunda DNA, lipidler, karbonhidratlar ve her çeşit başka kimyasal, canlılıkta görevlendirilmiştir. Forterre, RNA-virüslerin, DNA ve DNA eşlenme mekanizmalarının icadı gibi başlıca evrimsel geçişlerde önemli rol oynadığını düşünmektedir. Bu, ilk prokaryotik hücrelere ve en sonunda da bizim bildiğimiz canlılığa yol açmıştır.
"RNA Dünyası" hipotezine, ribozomun üç-boyutlu yapısının deşifre edilmesiyle birlikte büyük destek verildi; ribozomların önemli katalitik bölgelerinin RNA'dan oluştuğu ve proteinlerin ribozomal RNA'yı bir arada tutmada sadece yapısal bir rol oynadığı anlaşılmıştı. Özellikle belirtmek gerekirse, peptit bağının oluşumunun, amino asitleri proteinler şeklinde bağlayan tepkimenin RNA tarafından katalizlendiği artık biliniyor. Bu bulgu, RNA moleküllerinin büyük olasılıkla ilk proteinleri üretme yetisinin olduğuna işaretti.
Ancak, "RNA Dünyası" hipotezi mantıksız görünür çünkü günümüz dünyasında büyük RNA molekülleri içkin olarak kırılgandır ve hidrolizle kolayca bileşenlerine ayrılabilir. Hidroliz olmasa bile arka plan ışınımından RNA sonuçta parçalanır ve canlılık-öncesi Dünya'da çevresel koşullar oldukça zorlu idi. Kolayca hidrolize girmesi nedeniyle sitozinin makul bir canlılık-öncesi simülasyon yönteminin olmaması gerçeği ve canlılık-öncesi simülasyonlarda nükleotid oluşturma koşullarının şeker oluşturmanınkilerle uyumsuz olduğu gözlemi gibi çok sayıda başka kimyasal güçlük, pek çok bilimciyi, "RNA Dünyası" hipotezinin kimyasal açıdan gerçekçi olmadığını düşünmeye götürmüştür.
Proteinlere Daha Derin Bir Bakış
Proteinler, genlerin bilgisi ile biyolojik dünya arasındaki arayüzü meydana getirir. Dünya üzerindeki yaşamın evrensel yapısal birimleridir ve bir zamanlar, genetik bilginin aktarımını yapmada kilit yapı olarak DNA'nın tanımlanmasından önce, o işlevle ilgili olması en makul moleküller olarak görülmüşlerdir. Proteinlerin yapısı, işlevlerini belirler ve bir gendeki tek bir değişiklik, protein yapısının yüksek boyutlarını derinden etkileyebilir.
Proteinler, yapısal değişikliklere karşı çok hassastır. Önemli stratejik konumlarda yer alan amino asit dizilimleri, bir proteine işlevini belirleyen benzersiz yapıyı vermede son derece önemlidir. Üç-boyutlu uzayda ilişkili olan amino asitlerin kümeleri veya başka amino asit dizilimleri, önemli tanıma bölgeleri oluşturur. Proteinler, bir-boyutlu gen dizilimleri tarafından belirlenen bir-boyutlu amino asit dizilimlerinden inşa edilir. İlkesel olarak amino asitlerin kendilerini çok sayıda farklı şekilde yönlendirebilir olmalarına rağmen, onlar aslında sadece temelden farklı iki çeşit basit örüntü edinir. Bu iki-boyutlu örüntüler, alfa helezonlar ve beta yapraklar olarak bilinir. Tekil alfa helezonlar ve beta yapraklar, birincil amino asit diziliminin kısa parçaları tarafından birbirleriyle bağlantılandırılır. Yapısal öğelerin bu iki çeşidinin sayıları, bir proteinin ikincil yapısını; birbirleriyle bağlantı kurdukları kombinatoryal yol ise proteinin topolojisini tanımlar.
Birincil dizilim, protein yapısının daha yüksek boyutlu örüntülerini belirlemek için gereken tüm bilgiyi içerir. Her bir amino asit, ikincil yapının belirli çeşitlerinde görünme konusunda genel bir tercihe sahip gibi görünmektedir. Örneğin valin, izolösin, triptofan gibi bazı amino asitler en sık olarak beta yapraklarının içinde bulunurken; alanin, aspartat, glisin ve prolin gibi diğerleri çoğunlukla alfa helezonlarda bulunur.
Beta yapraklarının ve alfa-helezonal yapısal öğelerin kombinasyonları bükülerek, tutturularak ve birbirlerinin üzerine katlanarak, böyle daha yüksek boyutlu örüntüler ortaya çıkarabilir. Bu üç-boyutlu mimariler, proteinin üçüncül yapısı olarak bilinir. Bazı durumlarda, amino asit zincirleri yapısal heterojenlik sergiler ve iki ya da daha fazla alternatif üçüncül yapı arasında gidip gelir. Bazı proteinler, örneğin hemoglobin, birden fazla üç-boyutlu katlanmış amino asit diziliminin birleşiminden oluşur.
Bazı proteinler özdeş üçüncül yapı mimarilerine sahiptir ama topolojileri farklıdır. Topolojik varyantların varlığı, proteinlerin topolojik bir optimizasyon sürecinden geçtiklerine işaret eder. Üç-boyutlu uzayda özdeş dağılımlara sahip olabilirlerken, alfa ve beta yapısal öğelerinin farklı toplojik organizasyonlarının, proteinin katlanabilme ve böylelikle daha yüksek boyutlu uzaysal örüntülerini gerçekleştirebilme verimini etkilemesi muhtemeldir. Evrim, göreli katlanma verimlerine dayanarak topolojik varyantları seçmiş olabilir. Topolojik plastisite, potansiyel katlanmaların repertuarının maksimumda tutulmasını garantilemeye yardımcı olmuştur.
Şaperoninler (veya şaperonlar), üst üste duran çift-halkalı yapıyla karakterize edilen ve mitokondrilerde, ökaryotların sitozolünde, prokaryotlarda bulunan proteinlerdir. Şaperon (refakatçi) proteinlerin işlevi, diğer proteinlerin uygun katlanmayı başarmasına yardım etmektir. Çoğu şaperon, ısı şoku proteinidir (HSP); yani artan sıcaklıklara veya başka hücresel streslere yanıt olarak ifadelenen proteinlerdir. Bu davranışın nedeni, protein katlanmasının ısıdan şiddetli biçimde etkilenmesidir ve dolayısıyla bazı şaperonlar, yanlış katlanmanın neden olabileceği potansiyel hasarı onarma görevi yapar. Şaperonlar (veya şaperoninler), katlanma sürecinin bir kısmı sırasında hedef proteinle ilişkilendirilir. Ancak, katlanma tamamlanır tamamlanmaz (veya öncesinde bile) şaperon o anki protein molekülünü terk eder ve bir başkasının katlanışını desteklemeye gider.
Bir birincil dizilimin ortaya çıkarması muhtemel olan katlanmanın yapısını doğru şekilde öngörebilen güçlü algoritmalar artık var. Bu tür algoritmalar, sadece kısmen anlaşılmıştır ve bazı durumlarda, doğru katlanmayı tesis etmek için özelleşmiş şaperon proteinlerin ve foldaz enzimlerinin yardımı gereklidir. Başkaları sadece kalıcı bir kompleks oluşturdukları proteinler bağlamında doğru şekilde katlanır.
"Önce Peptit" Hipotezi
İlk yaşam formlarının, topluca otokatalitik peptit ağlarından oluştuğunu ileri süren hipotez, "önce peptit" hipotezi olarak adlandırılır. Eğer durum buysa, ilk iptidai peptit-bazlı canlılar, (1) ya kendini-eşlemeyen RNA molekülleri, (2) ya otokatalitik bağlama (ligasyon) tepkimeleri yoluyla kendini-eşleyen RNA molekülleri, (3) ya da şablon-bazlı bir eşlenme mekanizması kullanan otokatalitik olarak kendini-eşleyen moleküller tarafından sonuçta enfekte edilmiş olmalıdır.
Ferris ve ark. 55 amino asit uzunluğa kadarki p peptitlerinin, mineral yüzeylerde abiyolojik olarak sentezlenebileceğini göstermiştir. Daha uygun koşullarda, daha uzun peptitlerin de sentezlenebileceği tahmininde bulunmak makul olur. Katlanmış peptitler, 80 ilâ 100 amino asit uzunluklu ve sadece üç farklı amino asitten oluşan yapay olarak inşa edilmiş, rastgele kombinatoryal kütüphanelerde aşırı sık meydana gelir. 33 amino asitten daha kısa peptitler yüksek sıcaklıklarda istisnai kararlılığa sahiptir ve dikkat çekmeyen yapılara katlanabilirler.
Şablon-bazlı kendini-eşleme yolunda ilk adım, önceden-varolan kendini-düzenleyen peptit metabolizmasının, o noktada şablon-bazlı kendini-eşleme yapamayan, abiyolojik olarak sentezlenmiş RNA molekülleri tarafından enfekte edilmesi olmuş olabilir. Her ne kadar başlangıçta dijital dizilimlerinin içinde sembolik bilgi kodlamasalar da, bu RNA gen-öncülleri, gensiz peptit-bazlı proto-organizmaların spontane öz-düzenlemeli dinamiğini zorlamış ve yıkmış olabilir. Ayrıca ağ bileşenlerinin özelliklerini, örneğin katlanmalarına refakat ederek, kararlılıklarını artırarak veya etkinliklerini düzenleyerek modifiye edebilmiş de olabilirler.
Bununla birlikte, çoğu protein ısıya ve Dünya'nın erken dönemlerinde var olan koşulların çoğunda bozunmaya çok duyarlıdır. Bir diğer önemli nokta ise makromoleküler sistemlerde otokatalitik kendini-yapılandırmanın, yapısal bileşenler ile kendilerini sentezlemek için onların gerçekleştirdiği işlevsel operasyonlar arasında refleksif bir ilişkinin varlığını gerektirmesidir. Refleksiflik olasılığı, katalitik yapı-işlev ilişkisinin biçimsel, göstergesel özelliklerine bağlıdır; yani katalitik işlevlerin polimerik yapılar uzayına yerleştirilmesine bağlıdır. Refleksiflik, bazı genetik dizilimlerin göstergesel bir özelliğidir. Böyle dizilimler, seçme katalizörlerinin topluluğundaki otokatalitik öz-düzenlemenin bir sonucu olarak, kodlamanın evrimi için temel görevi görebilir. Otokatalitik seçilim, maddenin primitif biyokimyasal sistemlerde farklılaşmış hâle geldiği bir mekanizmadır. Kodlayan öz-düzenleme durumunda, simgesel bilginin yaratımına karşılık gelir. Wills'e göre, prionlar, otokataliz yoluyla eşlenmeleri, biyolojik göstergebilimin genetik kodlamadan daha az belirgin olan yönlerini yansıtan şimdiki zaman varlıklarıdır.
Prion Çıkmazı
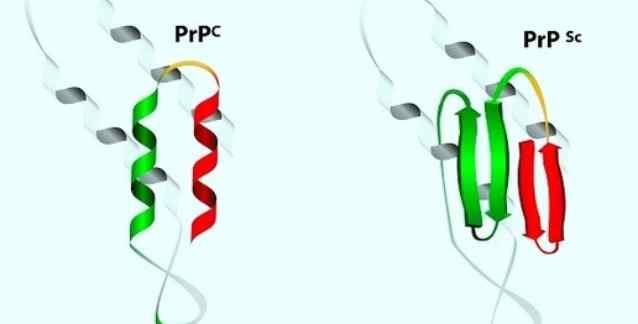
Süngerimsi beyin hastalıklarında aktarılan ve nükleik asitleri modifiye eden işlemlerle etkisizleştirilmeye direnç gösteren küçük proteinli bulaşıcı parçacıklar için Prusiner 1982 yılında "prion" adını önerdi. Prusiner, aktarılabilen etkenin nükleik asitten (DNA veya RNA'dan) yoksun olabileceğini ve sadece proteinden oluşuyor olabileceğini ileri sürdü. Sonrasında yapılan araştırmalar, prion hipotezini destekledi ve yüzyıllardır koyunlar arasında doğal olarak görülen bulaşıcı bir prionik hastalık olan Sıyırtma Hastalığına (İng. Scrapie) neden olan konak-kodlamalı bir proteinin anormal şekilde katlanmış bir izoformunun (PrP) karakterize edilmesine götürdü; PrPSc olarak gösterildi. Normal PrP protein, baskın bir asıl durum (PrPC) ile azınlıkta olan bir dizi başka biçim (konformasyon) arasında çalkalanır; bu biçimlerden biri ya da birkaçı kararlı bir supramoleküler yapı (PrPSc) oluşturmak için düzenli bir şekilde kendiliğinden-birleşme yapabilir. Kararlı supramoleküler yapı, otokatalitik bir oluşumla yanlış katlanmış PrP monomerlerden meydana gelir. İlginç bir şekilde, PrPC ile PrPSc arasındaki temel fark biçimseldir (konformasyoneldir).
Prionlar, prion proteinin baskın olan asıl durumunu (PrPC), işlevi bilinmeyen bir zar-ötesi glikoproteini, işlevsiz izomer (sıyırtma hastalığında PrPSc) ile değiştirerek, hayvanların ve insanların ölümüne yol açar. PrPC birincil olarak alfa helezonlardan, protein omurganın özel bir tür sarmal şeklinde büküldüğü bölgelerden oluşur. Ama PrPSc biçimi, omurganın tamamen genişletildiği bölgeler olan beta iplikleri içerir. PrPC ile PrPSc arasındaki temel fark biçimseldir. Anormal ve daha kararlı PrPSc izoformu, bir alternatif-katlanma yolağı sunar ve çoğunlukla nöronların ve lenfositlerin arasında birikir. Yayılım mekanizması, her iki izoform arasındaki fiziksel temasla ilgilidir. PrPSc formu, PrPC moleküllerine temas ederek ve onların katlanışının açılarak, otokatalitik bir tepkimeyle alışıldık biçimlerinden, sıyırtma hastalığı biçimininkine geçmesini sağlayarak kendini çoğaltır. PrP genindeki mutasyonlar, ortaya çıkan proteinlerin alfa-helezonaldan beta-yaprak şekline dönüşmeye duyarlı olmasını sağlayarak, eskiden normal olan konaklara da aktarılabilen bir genetik hastalık paradoksunu çözer.
Tüm prionların tehlikeli olmadığını vurgulamak önemlidir; aslında, prion-benzeri proteinler çok sayıda bitki ve hayvanda doğal olarak bulunur. Bu nedenle, bilimciler böyle proteinlerin konaklarına bir çeşit evrimsel avantaj verebildikleri çıkarımında bulunmuştur. Bir mantargil türü olan Podospora anserina için durumun öyle olduğu ileri sürülmüştür. Bu mantarın genetik açıdan uyumlu kolonileri birleşebilir ve besinler ile sitoplazma gibi hücresel içerikleri paylaşabilir. Yakın akraba olmayan koloniler arasında ayrımsız paylaşımı önlemek için koruyucu "uyumsuzluk" proteinlerinden oluşan doğal bir sistem vardır. HET-S adı verilen böyle bir protein, düzgün işlemek için prion-benzeri bir biçimi benimser. HET-S'nin prion formu, bir koloninin hücresel ağı boyunca hızla yayılır ve uyumlu koloniler birleştikten sonra proteinin prion-olmayan formunu bir prion durumuna çevirebilir. Ancak uyumsuz bir koloni, prion-içeren bir koloni ile birleşmeyi denerse, prion "işgalci"nin hücrelerinin ölmesine neden olarak, sadece yakın akraba kolonilerin kaynak paylaşımından yararlanmasını garantiler.
Onlarca yıldır, Saccharomyces cerevisiae mayasının (PSI+) denilen bir genetik özelliği, alışılmadık bir kalıtım örüntüsüyle tanımlanmıştır ve herhangi bir bildik mutasyon (PSI+) özelliğinden sorumludur. 1994 yılında Wickner, (PSI+) özelliğinin ve bir diğer anormal kalıtımlı özellik olan (URE3) özelliğinin bazı normal hücresel proteinlerin prion formlarının sonucu olduğu hipotezini öne sürdü. HSP, (PSI+) ve çok sayıda başka maya prionunun kalıtım ve aktarımına incelikle bağlıydı. O zamandan beri, araştırmacılar (PSI+) ve (URE3) için kodlama yapan proteinlerin nasıl prion ve prion-olmayan formlar arasında dönüşüm yapabildiğini ve ayrıca hücreler-arası prionlara sahip olmanın sonuçlarını açığa çıkardı. Bazı zararlı koşullara maruz kaldığında, aslında (PSI+) hücreleri prionu-olmayan kardeşlerinden daha iyi işliyordu; bu bulgu bazı proteinlerde bir prion formu edinme yetisinin, pozitif evrimsel seçilimden ortaya çıkabileceğine işaret etti. Prion bulaşmış ve prionsuz formlar arasında dönüşüm yetisinin, mayanın hızla ve tersinir şekilde değişken ortamlara uyumlanmasını sağladığı tahmin edildi.
Tüm mevcut kanıtlar, geniş bir çeşitlilikteki temel biyolojik süreçleri, prionların epigenetik olarak modüle ettiğine işaret etti. Onlar, Mendelyen-olmayan bir yolla kalıtılan çok sayıda fenotipin kökenindelerdir.
Prionlar ve İlk Canlılığın Belirişi
Dünya üzerinde ilk canlılığın belirişi hâlâ tartışmalı bir konudur. Pek çok nedenden ötürü, DNA ve RNA bu ilk işlev için pek uygun değildir. Onların yüksek kimyasal karmaşıklığı, abiyotik bir ortamda sentezlenmelerinin önünde çok sayıda kimyasal engel olması ve modern çağ nükleik asitlerinin Dünya'nın erken dönemlerindeki zorlu koşullara karşı çok duyarlı olması, çoğu bilimciyi başka olasılıklar aramaya itti.
Chien ve arkadaşlarına göre, mantargillerdeki Mendelyen-olmayan çeşitli özelliklerin, protein konformasyonundaki kalıtılabilen değişikliklere (ki bunlar bazen yararlı olabilir) bağlı olduğunun bulunmasıyla, prion hipotezi genişletilmiştir. Hücresel kofaktörlerin spesifik rolü hakkında öğrenilecek daha çok şey olmasına karşın, memeli ve maya prion görüngüleri arasındaki mekanistik paralellikler, genellikle amiloid denilen düzenli beta-yaprağı-zengini protein birikimlerinin yayılımı ile ilgili olan konformasyon-bazlı enfeksiyonun ve kalıtımın evrensel özelliklerine işaret eder. Wickner ve ark. amiloid-benzeri birikimlerin fiziksel özellikleri cinsinden, prionların daha iyi açıklanabileceğini düşünmektedir. Kimyasal açıdan özdeş bulaşıcı parçacıkların oluşturduğu prion suşları, ayrık fenotiplere neden olur ve sıklıkla farklı türler arasında prion aktarımını önleyen engeller olur. Bunların ikisinin de aynı görüngünün farklı yüzleri olduğuna işaret eden kanıtlar artmaktadır: Bir proteinin çok sayıda kendini-çoğaltan konformasyonlara yanlış katlanma yetisi. Tekil mutasyonlar bile yeğlenen yanlış katlanmış konformasyonların izgesini değiştirebilir. Karşılığında, amiloid konformasyonundaki değişiklikler, çoğalmanın spesifikliğini ve suş fenotiplerini değiştirebilir. Bu model, prion kalıtımının çok sayıda yaygın ve diğer türlü kafa karıştıran özelliğinin yanı sıra, toksik yanlış katlanmış proteinlerle ilgili olan bulaşıcı-olmayan hastalıkların çeşitli yönlerini açıklamaya yardım eder.
Chernoff, prionların hem memelilerdeki bulaşıcı hastalıkların, hem de mantargillerdeki kalıtılabilen özelliklerin sorumlusu olan, kendini-sürdüren protein izoformları olduğunu belirtmiştir. Bilinen çoğu prion proteinler, amiloidler (öz-tohumlamalı, lif-benzeri birikimler) oluşturur. Prion yayılımı ("eşlenme"), birikimin "makaslanarak" küçük tohumlara dönüştüğü, sonra bu tohumların büyüyerek tam boyutlu polimerler olması şeklindeki yinelenen çevrimlerin bir dizisi olarak tanımlanabilir. Birikimler oluşturma ve onları yayma yetisi, kompozit prion alanlarının ayrı bölgeleri (PrD) tarafından kontrol edilir.
Amiloidler, öz-toplanımlı lif-benzeri beta-zengini protein birikimleridir. Amiloidojenik prion proteinler, amiloid durumu in vivo yayar ve onu bulaşma yoluyla veya hücre bölünmelerinde iletir. Amiloid birikimi herhangi başka bir proteinin yokluğunda olabilirken, amiloid durumun yayılımı, şaperon yardımcıları gerektirir. Maya prion proteinleri, ilgili işlevlerden sorumlu olan ayrık birikim ve yayılım öğelerine sahip prion bölgeleri içerir. Bilinen birikim ve yayılım öğelerinin uzunlukları kısadır ve nispeten basit dizilimlerden oluşurlar ki bu da onların olası antik orijinlerine işaret eder. Chernoff'a göre, prion-benzeri öz-toplanımlı yapılar, yaşamın başlangıcındaki biyolojik bölümlenmenin (kompartımanlaşmanın) ilk adımlarıyla ilgili olabilir.
Bousset ve Melki, Mendelyen-olmayan bir biçimde kalıtılan çok sayıda fenotipin kökeninde olduklarını düşünmüştür. Prionlar, bu yapı-bazlı kalıtımın kökenindeki moleküler olayları mercek altına almak için çok kullanışlıdır. Geçen yarım yüzyıl boyunca biriken deneysel kanıt, kalıtılan varyasyonun, genomik dizilimlerdeki değişikliklerle sınırlı olmadığına açıkça işaret etmiştir. Prion modeli, başlangıçta memelilerdeki bazı nörodejeneratif hastalıkların sıradışı aktarımını temel alarak, alternatif protein konformasyonlarının şablon-benzeri üremesi için bir moleküler mekanizma sağlamıştır. Mayada ve diğer mantargillerde bu modeli protein-bazlı genetik öğelere genişleten son veriler, mayanın protein-bazlı genetik öğelerinin çoğalmasının ve aktarımının, hücrenin "prion eşleme" mekanizması (protein yapıların ve multiprotein komplekslerinin toplanması ve dağılması süreçlerinden sorumlu protein yardımcılardan oluşur) tarafından kontrol edildiğini açığa çıkarmıştır. Bunların arasında, stresle ilgili şaperonlar olan HSP100 ve HSP70 grupları önemli bir rol oynar. Bu proteinlerin düzeylerinde veya etkinliklerindeki değişimler, protein-bazlı genetik elemanlara göre "mutator" veya "antimutator" etkilerle sonuçlanır. Prion oluşturma yetileri, karşılık gelen amino asit dizilimlerinin ıraksamasına karşın, evrimde korunmuş görünmektedir. Dahası, kökenleri farklı olan geniş çeşitlilikteki proteinler, belirli koşullarda potansiyel olarak prion-benzeri değişimlerle sonuçlanabilecek olan amiloid-benzeri birikimler oluşturma yetisi taşıyor görünmektedir.
Rode ve ark. prionların peptit evriminin erken evrelerinin bir kalıntısı olma olasılığını analiz etti. Prionlar nispeten küçük olan proteinli bileşikler olup, morötesi ve iyonlaştırıcı ışınıma karşı çok dirençlidir. Kimyasal kararlılıklarına, jeokimyasal verilere ve ilkel dünyadaki en olası çevresel koşullara dayanarak, kimyasal evrim tarafından peptitlerin ve proteinlerin, polinükleotidlerden çok daha önce üretildiği varsayılmalıdır. Bilinen prionlarda en sık görülen amino asit dizilimleri ile tuz-tetiklemeli peptit oluşum tepkimesinde tercihan oluşan dizilimin (ilkel dünya koşullarında peptitlerin oluşmasına olanak tanıyan en basit mekanizma) basit bir kıyaslaması, dikkat çekici bir tutarlılık sergiler; bu da, prionların erken evre peptit evriminin bir kalıntısı olduğu hipotezini destekler. Canlılık, bugün bildiğimiz yaşam formlarının modern genetik mekanizmaları gelişmeye başlamadan önce, aslında proteinle ilgili bir temelle başlamış olabilir; DNA/RNA bazlı evrim, evrimin ilk adımı değil de, daha çok son adımı olmuş olabilir. Ancak böyle yavaş ve daha verimsiz bir yaşam çeşidi, yeni beliren RNA/DNA bazlı mekanizma tarafından çabucak elimine edilirdi ve varlığı sadece günümüzde mantargillerdeki bazı garip epigenetik modülasyonlarda ve memelilerdeki süngerleştirici beyin hastalıklarında fark edilebilirdi. Belki de prionlar, günümüzde nükleik asitler tarafından temsil edilen dijital koddan farklı olarak, biyolojik bilgi aktarımının çok eski bir analog kodunu temsil ediyor olabilir.
Her protein veya polipeptit zincirinde, özel bir şekilde dizilmiş amino asitler bulunur. Amino asitlerin diziliş sırası, büyük ölçüde proteinlerin biyolojik ve fizikokimyasal özelliklerini belirler. Proteinlerin amino asit sıralarının belirlenmesinde çok gelişmiş yöntemler mevcuttur. Bu bilgi ile basit proteinleri ve 51 amino asit içeren insülin hormonu gibi polipeptitleri kimyasal olarak sentezlemek mümkündür. Biyolojik aktivite, aynı zamanda, polipeptit zincirlerinin uzaydaki (boşluktaki/ üç boyuttaki) düzenlemesi ile de ilgilidir. (Polipeptit burada bir "peptit polimer bağları ile bağlı" biyo-polimer zincirini belirtmek için sıfat olarak kullanılmıştır.) Polipeptit zincirinin boşluktaki düzenlemesine molekülün şekli denir.
(...)
Bir protein zincirinde amino asitlerin dizisi, onun primer yapısı olarak bilinir. Protein moleküllerinin, kovalan ve nonkovalan güçlerle stabilize edilen ve tersiyer yapı olarak adlandırılan bazı üç boyutlu şekillerde olduğu varsayılır. Tersiyer yapı, sekonder yapının parçalarından oluşmuştur ve gelişigüzel bölünen alfa-heliks veya kırmalı tabaka gibi parçalarla tanımlanır. En son olarak, bazı proteinler, basit protein alt-birimlerinin bir araya gelmesiyle oluşmuştur; böyle bir düzeydeki organizasyon quarterner yapıdır. Daha önceki organizasyon ve yapı özelliklerini (örn. sekonder ve tersiyer yapı) ayırt etmek bazen zordur.
(...)
Canlı hücrelerdeki veya maksimum biyolojik aktivite gösteren izole edilmiş proteinlerdeki şekil "olgunlaşmış durum" olarak adlandırılır. Olgunlaşmış durumdaki bir protein, en iyi işlev görür.
(...)
Bir protein molekülünün olgunlaşmış durumu ve protein zincirinin boyutsal anlamda tam olarak gelişigüzel durumu arasında, birçok şekil vardır. Bütünüyle gelişigüzel olduğu şekilde, proteinin tam olarak denature olduğu söylenir.
– Montgomery & Conway & Spector & Chappell (Biyokimya: Olgu Sunumlu Yaklaşım, ISBN: 9789757477679)
- Are prions related to the emergence of earlylife? http://www.santacasadermatoazulay.com.br/wp-content/themes/david_azulay/site-antigo/trabpub/are_prions_related_to_the_emergence_of_early_life.pdf
Dilediğiniz miktarda aylık veya tek seferlik bağış yapabilirsiniz.
Destek OlBunlar da İlginizi Çekebilir