Mikroplar Alzheimer Hastalığını Tetikliyor Olabilir mi?
2011 yılının sonlarında, Drexel Üniversitesi cildiye profesörlerinden Herbert Allen, ölen Alzheimer hastalarının beyinlerinde spiroketler (İng. spirochete) adı verilen, uzun sar...
 Kirstypargeter /iStock
Kirstypargeter /iStock
Yıldız Teknik Üniversitesi - Çevirmen/Editör

2011 yılının sonlarında, Drexel Üniversitesi cildiye profesörlerinden Herbert Allen, ölen Alzheimer hastalarının beyinlerinde spiroketler (İng. spirochete) adı verilen, uzun sarmal tirbuşon şeklindeki bakterilerin varlığını ortaya koyan bir makaleye rastladı. Daha önce yayımlanmış raporları derleyen Uluslararası Alzheimer Merkezi araştırmacısı Judith Miklossy ve ekibi, 495 Alzheimer hastasından 451 tanesinin beyninde spiroket bakterileri olduğuna ilişkin kanıtlar bulmuştu. Vakaların %25'indeki spiroket bakterilerinin Borrelia burgdorferi türünde olduğu saptandı; yani Laym (İng. Lyme) hastalığına neden olan bakteriydi. Kontrol grubu beyinler ise spiroket barındırmıyordu.
Bu çalışma, Allen'ı 40 yıl önceyi hatırlamaya sevk etti. Johns Hopkins Üniversitesi'nde stajyer olduğu sıralarda, demansı da içeren nörolojik bir sendrom olan "nörosifilis" tanısı konmuş bir hastası olmuştu. Sendrom, beynin sifilis spiroketlerinin işgaline uğraması sonucunda oluşuyordu. "Laym hastalığı ile sifilis arasındaki benzerlik bana çok ilginç gelmişti," diyor Allen.
Allen, kısa bir süre önce, egzamada biyofilmlerin (yüzeylere yapışan ve bağışıklık saldırılarına da, antikorlara da çok dirençli olan bakteri kolonilerinin) payı olabileceğine ilişkin yeni bir olasılık öne sürdü. Biyofilmler cilt kanallarını tıkadığı ve içsel bağışıklık yanıtlarını tetiklediği için inatçı cilt sorunlarına yol açabileceğini söyledi. Allen, Laym spiroketlerinin biyofilm oluşturduklarını gösteren çalışmalardan haberdardı. Bu da onun, biyofilmlerin Alzheimer hastalığında da rol oynayıp oynamadığını merak etmesine neden oldu. Ölen Alzheimer hastalarının beyinlerindeki biyofilmlerin konumlarına bakan Allen, amiloid plakları ile aynı hippokampal yerlerde olduklarını gördü. Toll-benzeri almaç 2 (TLR2) adı verilen önemli içsel bağışıklık elemanının da, Alzheimer'lı beyinlerin aynı bölgesinde bulunduğu, fakat kontrol grubu beyinlerde olmadığı saptandı. Allen, TLR2'nin bakterilerin varlığı dolayısıyla etkinleştiğini, fakat biyofilmler nedeniyle içeride sıkıştığından, çevresindeki dokuya zarar verdiği varsayımını ileri sürdü.
 Alzheimer'lı insan beyninin hippokampal bölümündeki biyofilmler ve amiloid-β görülüyor. (COURTESY OF HERBERT ALLEN)
Alzheimer'lı insan beyninin hippokampal bölümündeki biyofilmler ve amiloid-β görülüyor. (COURTESY OF HERBERT ALLEN)
Ağız mikrobiyomunun alışıldık bir üyesi olan spiroketler, kan dolaşımında olduklarında (örneğin aktif Laym enfeksiyonlarında veya ağız ameliyatından sonra) kan-beyin engelini aşabilen az sayıdaki mikroptan biridir. Ancak, bu bakteriler o kadar yavaş bölünür ki, bir biyofilm oluşturmaları onlarca yıl alabilir. Bu durumun, Alzeimer hastalığının bir yaşlılık hastalığı olmasıyla örtüştüğünü düşünen Allen, sifilis vakalarının da (spiroketlerin nöroinvazif etkileri, birincil enfeksiyondan 50 yıl kadar sonra ortaya çıkabiliyor) bunu kuvvetlendirdiğini belirtiyor.
Allen'ın çalışması, Alzheimer hastalığının gelişimi ile ilgili uzun süredir bir köşeye atılmış hâldeki bir hipotezi diriltti. 30 yıldan bu yana, patojenik mikropların, hastalığın nöropatolojisini tetikleyebileceği olasılığını araştıran bir avuç bilimci var. Bu kişilerin çoğu, söz konusu bağlantıya şans eseri rastlamış; tıpkı Allen gibi. Onca eleştiriye ve tüm o kaynak bulma ve yayın yapma sorunlarına rağmen, bazıları hayatını bu konuya adamış. Miklossy, zaman içinde çok sayıda gözlem birikmesine rağmen, kendisine aptal gözüyle bakıldığını ve kaynak sağlanmadığını anlatıyor. Yine de spirochetes'in Alzheimer hastalığında payının olup olmadığını araştırmaktan vazgeçmemiş. "Ben Hipokrat Yemini etmiş bir doktorum. Elimizden ne geliyorsa yapmamız gerek," diyor.
Şimdilerde Alzheimer alanında çalışan bilimciler, hastalığın doğuşunu açıklayabilecek bir kuram peşinde. Bilimciler hâlâ hastalığın hangi özelliklerinin, hastalığın ilerleyişi ile ilgili olduğunu kesin olarak söyleyemiyor: Nöroenflamasyon mu, tau düğümleri mi, amiloid plakları mı? Bu netleştirilmediği için de tedavi için işe yarar hedefler belirlenemiyor. Şu ana dek, klinik teste sokulan ilaçların çoğu amiloid-beta peptitini (Alzheimer'lı beyinlerin karakteristiği olan amiloid plaklarının ana bileşenini) hedef alan ilaçlar oldu. Amiloid-beta birikiminin nöropatolojiye yol açtığı ve dolayısıyla amiloid-betanın olmamasının (üretimi azaltılarak, yayılımı azaltılarak veya molekülün beyinden atılmasına yardım edilerek) demans belirtilerini azaltabileceği ya da en azından artmasını engelleyebileceği düşünüldü. Fakat şimdilik araştırmacıların eli boş kaldı.
Örneğin Kasım 2016'da, Eli Lilly'nin (ABD merkezli bir ilaç firması) amiloid hedefli antibiyotiği "solanezumab"ın Faz 3 denemesi, erken evredeki hastalarda iyileşme sağlamadı. Bu pahalıya mal olan ve yıkıcı bir başarısızlıktı. Birkaç ay sonra olayın bir benzeri daha gerçekleşti. Merck (bir başka ABD merkezli ilaç firması), amiloid-beta üreten enzimi bloke eden "verubecestat" adlı küçük-molekül ilacının klinik denemelerini sonlandırdı.
Bunlar, Alzheimer için geliştirilen ve klinik denemelerde hiçbir yararı görülemeyen deneysel ilaçlar zincirine eklenen son iki üyeydi. Denemeleri suçlayanlar da var. Moleküler nörolog John Hardy, klinik denemelerde kalitenin düşük olduğunu söylüyor. Azıcık ilacın daha beyne varış bile yapamadığını vurguluyor. Bazı araştırmacılar ise ilaçların temelindeki kuramı sorguluyor. Etkin ilaçların geliştirilmesinde süregiden başarısızlıkların ışığında, hastalığa ilişkin alternatif kuramların üretilmesi için çaba gösterilmesi gerektiğini düşünenler var. "Bence Alzheimer hastalığı ile ilgili hipotezlerin, amiloid plakları, düğümler ve inflamasyonun yanı sıra, enfeksiyonu da içermesi gerek," diyor Harvard nörobiyologlarından Rudolph Tanzi.
 Bakteriyal veya viral enfeksiyonlar ile Alzheimer hastalığının nöropatolojisi arasındaki bağlantıya ilişkin kanıtlar artıyor. © KIMBERLY BATTISTA
Bakteriyal veya viral enfeksiyonlar ile Alzheimer hastalığının nöropatolojisi arasındaki bağlantıya ilişkin kanıtlar artıyor. © KIMBERLY BATTISTA
Herpes simplex virüsü tip 1 (HSV1), beyni şiddetli şekilde enfekte edebilir ve ender görülen çok ciddi bir beyin iltihabına yol açabilir. 1980’lerin sonlarında, Manchester Üniversitesi’nden moleküler virolog Ruth Itzhaki, HSV1 hastalarında etkilenmiş beyin bölgelerinin, Alzheimer hastalarında hasar almış beyin bölgelerinin aynısı olduğunu fark etti. Herpes'in vücutta uzun süreler boyunca belirti vermeden saklanabileceğini bildiğinden, enfeksiyon ile nörodejeneratif bozukluk arasında nedensel bir bağlantı olabileceği Itzhaki'nin aklına geldi.
Alzheimer hastalarının beyinlerinde HSV1 DNA'sı aramaya başlayan Itzhaki, aradığını buldu. Fakat bu viral DNA, aynı yaşlardaki kontrol grubu beyinlerde de mevcuttu. O zamanlar yeni bir teknik olan PCR (polimeraz zincir tepkimesi) kullanmak zorluklarla doluydu ve Itzhaki'nin bulgularına kontaminasyon (bulaşma/kirlenme/safsızlık) kaynaklı denilerek meydan okunuyordu. Itzhaki çalışmasını büyük bir titizlikle yineledi. İleri yaştaki insanların, Alzheimer olsunlar ya da olmasınlar, üçte ikisi ilâ dörtte üçünün beyinlerinde HSV1 olduğunu yine buldu.
Ardından, neden HSV1 bulaşmış bireylerin sadece bir kısmında demans geliştiğini açıklamak için genetik farklılıkları incelemeye başladı. Sonunda 1997 yılında, beyinde hem HSV1 hem de apolipoprotein E gen varyantı APOE4 taşıyor olmanın, ele aldığı Alzheimer vakalarının %60'ını açıklayabildiğini rapor etti; her iki etkenin tek başına yapabildiğinden çok daha yüksek bir orandı bu. Ama Alzheimer araştırmacılarının çoğu, Itzhaki'nin çalışmasını yine gözardı etti. Onların kendi düzenlerini kurmuş olduklarını ve plaklar ile düğümleri içeren senaryolara fazlasıyla bağlandıklarını belirtiyor Itzhaki. "Virüsler hakkında bilgileri yok; özellikle de herpes virüsünün bedende ve beyinde saklı kalabileceğinden. Virüsün bir şeye neden olabileceği söylendiği anda, senaryonun çok hızlı gelişeceğini düşünüyorlar. Bu çok safça bir düşünce," diyor.
Aynı sıralarda, o dönem İsviçre'deki Lozan Üniversitesi'nde olan nöropatolog Miklossy, hem nörosifilis, hem de Laym bakterilerinin neden olduğu bir sendrom olan nöroborelya için spiroket kaynaklı beyin hasarını detaylandırıyordu. Bakteriyal işgal ve plak oluşumu kanıtı sunan bir kafa travması vakasına denk geldi ve dikkatini Alzheimer'a yöneltti. 14 tane Alzheimer hastasının beyin dokularından spiroket yalıtırken, 13 tane aynı yaştaki kontrol grubu beyinlerde hiç spirokete rastlamadı. Buna ek olarak, amiloid öncü proteinini (APP, yani amiloid öncü proteini bölündüğünde amiloid-beta oluşturur) hedef alan monoklonal antikorların , bulunan spiroket türleri ile çapraz tepkimeye giriyordu; ki bu da bakterilerin, proteinin kaynağı olduğuna işaret ediyordu. 1993'te yayımladığı bulgularına biraz olumlu tepkiler alabilmesine rağmen, Miklossy de tıpkı Itzhaki gibi kuşkuculuktan payına düşeni aldı. Çalışmasına yapılan eleştirilerde "aptalca, doğru bilinene aykırı ve çılgınlık," gibi yorumlar da olduğunu anlatıyor.
Bu arada ABD'de, Alzheimer ile mikrobiyal enfeksiyon arasında bağlantı olabileceğine ilişkin üçüncü bir kanıt dalgası oluşmaya başlamıştı. MCP Hahnemann Tıp Okulu mikrobiyologlarından Alan Hudson, bir dolandırıcılık araştırma komitesinde görev yaparken Brian Balin ile tanıştı. Çok geçmeden nöropatolog Balin, Hudson'a Alzheimer'lı beyin dokuları göndermeye ve hücre içinde Chlamydia cinsinden bakterilerin olup olmadığını sınamasını istemeye başladı. Bazı örneklerde C. pneumoniae için test pozitif çıktı. Bakteriler, Alzheimer nöropatolojisi ile ilişkilendirilen beyin bölgelerindeki (hippokampus ve diğer limbik sistem alanlarındaki) mikroglia ve astrositlerde bulunuyordu. Hudson, sonuçları Balin'e bildirmeden önce testleri bir başka teknisyene daha tekrarlattı. Negatif çıkanların hepsi kontrol grubu beyinler iken, pozitif çıkanların hepsi Alzheimer'lı beyinlerdi. "Ağzımız açık kaldı," diyor Hudson. Bulgularını duyurdukları makaleyi yayımladıklarında, Balin, Hudson ve çalışma arkadaşları dünya basınında yer buldu. Ama Alzheimer araştırmacıları toplantısına katıldıklarında, kendileri ile kimsenin muhattap olmadığını söylüyor Hudson.
Böylece 1990'larda, farklı organizmaları inceleyen ve farklı ülkelerde bulunan üç laboratuvar, Alzheimer hastalığının nedenleri arasında insan patojenlerinin olabileceğine ilişkin işaretlere sahip olmuş oldu. Kuramcılar için ise Alzheimer hastalığının mikrobiyal enfeksiyon bileşeni olabileceği düşüncesi hâlâ kabul edilemezdi.
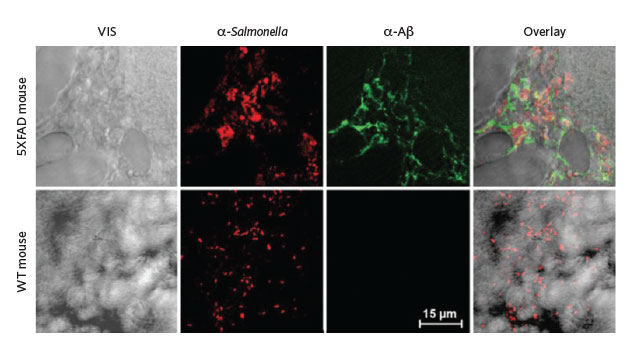 Transjenik fareler (en üst sıra), beyinlerine Salmonella girdikten 48 saat sonra, ilgili bölgelerde yüksek düzeyde amiloid-beta oluşturdular. (REPRINTED WITH PERMISSION FROM D.K.V. KUMAR ET AL., SCI TRANSL MED, 8:340RA72, 2016.)
Transjenik fareler (en üst sıra), beyinlerine Salmonella girdikten 48 saat sonra, ilgili bölgelerde yüksek düzeyde amiloid-beta oluşturdular. (REPRINTED WITH PERMISSION FROM D.K.V. KUMAR ET AL., SCI TRANSL MED, 8:340RA72, 2016.)
2016 yılında Itzhaki, Miklossy, Hudson, Balin ve 29 başka bilimci daha, mikropların Alzheimer hastalığının oluşumundaki katkısına işaret eden kanıtları derledikleri bir makaleyi, Journal of Alzheimer’s Disease dergisinde yayımladı. Makalenin başında şöyle bir çağrı vardı: "Bizler, Alzheimer hastalığı üzerinde çalışan araştırmacılar ve klinisyenleriz . . . ve hastalığın bir yönünün görmezden gelinmesi konusundaki kaygımızı ifade etmek için yazıyoruz."
Derginin editörü olan ve Texas Üniversitesi'nde araştırmalarını sürdüren George Perry, makalenin basılmasını kabul etmenin yanı sıra, yazar olarak da imzasını atmış. "The Journal of Alzheimer’s Disease dergisi, her türlü farklı düşünceye açık. Biz popülariteyi önemsemiyoruz," diyor Perry.
Yavaş ve emin adımlarla, Alzheimer araştırmacıları sonunda patojen hipotezini derinlemesine incelemeye karar vermiş gibi görünüyor. En yeni mikrobiyal kuramcılardan Tanzi, Alzheimer alanında onlarca yıldır öne çıkan bir isim. 1987 yılındaki APP geni keşfine (keşfedilen ilk Alzheimer bağlantılı gen) katkıda bulunmuştu. Yakın zamanda, Tanzi ve çalışma arkadaşları, amiloid-beta'nın deney tüpünde patojenik bakterilerin (Candida albicans, E. coli ve Staphylococcus aureus dahil) çoğalmasını engellediğini gösterdi. Bu da, Alzheimer ile ilişkilendirilen bu peptitin, antimikrobiyal görevi gördüğüne işaret ediyor.
Tanzi'nin işleyiş hipotezi şöyle: Mikroplar, içsel bağışıklık tepkisi tetikliyor ve amiloid-beta bunda kilit rol oynuyor. Peptit, sağlıklı dokuyu işgalcilerden korumak için enfeksiyon bölgesine duvar örüyor. Fakat çok miktarda yığılma olduğunda da, bundan dolayı (örülen koruyucu duvarlardan dolayı) sorunlar çıkmaya başlıyor. Plaklar, nöron ölümlerine yol açmaya başlıyor.
Tanzi'nin ekibi tarafından yapılan bir diğer çalışmada, amiloid-beta'nın mikroplara tutunduğu ve diğer amiloid-beta'lara bağlanarak, işgacileri kapana kıstırdığı, böylece onların konak hücre ile etkileşmelerini engellediği ortaya kondu. Kuşkusuz, Alzheimer hastalığının transjenik bir fare modelinde, Salmonella enfeksiyonu beyindeki amiloid plaklarının temelini atmıştı. "Plaklar, hippokampus ve temporal kortekste üretilmişti; buralar, kan-beyin bariyerinin aşılmasına en açık bölgelerdir," diyor Tanzi. Buraların, patojenlerin girmeyi başardığı ilk yerler olduğuna işaret ediyor.
Tanzi, Miklossy'nin ve diğerlerinin aldıkları eleştirilerin farkındaydı. Kendi alacağı eleştirileri de bekler vaziyette şunları söylüyordu: "Her şeyi doğru yapmaya çalıştık, tüm kontrolleri yaptık. Bu makale üzerinde sekiz yıl çalıştık." Fakat onu şaşırtan bir şekilde, çok fazla olumsuz tepki gelmedi. Alzheimer araştırmacılarının sonunda mikrop kuramı üzerinde düşünmeye başladıklarının bir göstergesi olsa gerekti bu.
 Alzheimer nörodejenerasyon patolojisi ile enfeksiyon arasındaki bağlantıyı açıklamaya çalışan çeşitli hipotezler bulunuyor. © KIMBERLY BATTISTA
Alzheimer nörodejenerasyon patolojisi ile enfeksiyon arasındaki bağlantıyı açıklamaya çalışan çeşitli hipotezler bulunuyor. © KIMBERLY BATTISTA
Ama yine de bu düşüncenin taraftarları kuşkuyla karşılanıyor. New Mexico Sağlık Bilimleri Merkezi'nden moleküler nörobiyolog Elaine Bearer, HSV1 ile Alzheimer nöropatolojisini bağlantılandıran çalışmasını sunduğunda karışık tepkiler almış. Bearer'in temel araştırma konusu, moleküler motorların dev kalamar aksonda kargoyu nasıl teslim aldıkları ve deneysel kargo olarak da HSV1 kullanıyor. Çünkü HSV1'in aksonal ulaştırma rotaları boyunca her iki yönde de seyahat ettiği biliniyor. Enfeksiyon sırasında, HSV1 duyusal sinir uçlarından sinir hücresinin kendisine gidiyor ve burada saklanabiliyor. Etkinleştiğinde, HSV1 tekrar sinapslara dönüyor, epitelyal hücreleri yeniden enfekte ediyor ve işte: Yine bir uçuk!
Bearer 2006 yılında, HSV1'in aksonal ulaştırma mekanizmasına tutunmak için APP kullandığını buldu. Bunun sonucunda, HSV1 APP'yi nöron içine yeniden dağıtıyordu. Yani APP, enfekte olmamış hücrelerde gerçekleşmeyen yollarla birikebiliyordu. Kısa bir süre önce de virüsün APP'ye "bir şeyler yaptığı" anlaşıldı. "Epitelyal hücrelerde, proteinde 25 kat artışa neden oluyor," diyor Bearer. Bu da, proteinin sentezinin enfeksiyona da yanıt verdiğini akla getiriyor.
Bearer ayrıca HSV1'in insan beynindeki amiloid plaklarında kıstırıldığına ilişkin kanıtlar da ortaya koydu. Bu çalışmasının sunumunu yaptı, fakat Eylül 2017 itibariyle henüz yayımlanmış değil. Elde ettiği bulgular, Tanzi'nin bir hayvan modeldeki amiloid plaklarının içinde bulduğu Salmonella bulgusu ve Allen'ın insan beyin dokusundaki amiloid-beta ile aynı yerdeki bakteriyal biyofilm bulgusu ile uyuşuyor.
Alzheimer hastalığını mikrobiyal kuramını destekleyen kanıtlar artmasına rağmen, bu yöndeki çalışmalar için finansman bulmak hâlâ kolay değil. Yaklaşımı eleştiren bilimci sayısı da hâlâ çok fazla. Örneğin mikrobiyal kurama ikna olmadığını belirten Hardy'nin itirazları şunlar: Birincisi, mikropların Alzheimer nöropatolojisine neden olması fikri, hastalığın kalıtımsal yönünü açıklamıyor. Ayrıca plakların ve düğümlerin hasta beyinlerdeki karakteristik anatomik dağılımını da açıklamıyor. Hardy, kan kaynaklı hastalıkta, dağılımın beyinde daha yaygınlaşmış durumda olması gerektiğini düşünüyor. Durumun epidemiyolojiye, nöropatolojiye ve genetiğe uygun düşmediğini söylüyor. Düşüncesini değiştirmesi için daha fazla deneysel kanıt talep ediyor. Neden-sonuç ilişkisini açıkça gösteren deneyler yapılmasını istiyor: Fareyi enfekte edin ve hastalığı gösterin, diyor.
Mikrop kuramcıları, önerdikleri mikrobik tetiklemenin, Alzheimer'ın tek nedeni olmadığını söylemekten çekinmiyor. Itzhaki'nin çalışmasında, vakaların %40'ı HSV1 enfeksiyonu ile açıklanmıyordu. Elbette Alzheimer'ın enfeksiyon ile bağlantılı olması fikri, belli tek bir patojen ile sınırlı değil. Hipotez şundan ibaret: Enfeksiyonun ardından, bazı patojenler beyne sızıyor. Burada tetiklenen bağışıklık tepkisi sonucunda, amiloid-beta birikimi başlıyor ve plak oluşumu gerçekleşiyor.
Alzheimer hastalığına ilişkin, şu anda elimizde yanıttan çok, soru var. Başarısızlığa uğrayan çok sayıda ilaç var ve Alzheimer'a neden olan etkenler net olarak belirlenemiyor. Bilimcilerin inceleyebildiği örneklerde, hastalık hep çok ilerlemiş oluyor. Beynin sonuçta ne hâle geldiğine bakıp, onu o duruma getiren süreci tahmin etmek ise kolay olmuyor. Bilinen bir şey var ki, amiloid bu hastalıkta önemli. Ama hastalığın merkezinde olan ile hastalığın nedeni olan şeyler her zaman aynı olmuyor. Dünyanın her yanından binlerce araştırmacı tarafından gece-gündüz üzerinde çalışılan bu hastalığa bir an önce çare bulunmasını umuyoruz.
Bu çalışma, Allen'ı 40 yıl önceyi hatırlamaya sevk etti. Johns Hopkins Üniversitesi'nde stajyer olduğu sıralarda, demansı da içeren nörolojik bir sendrom olan "nörosifilis" tanısı konmuş bir hastası olmuştu. Sendrom, beynin sifilis spiroketlerinin işgaline uğraması sonucunda oluşuyordu. "Laym hastalığı ile sifilis arasındaki benzerlik bana çok ilginç gelmişti," diyor Allen.
Allen, kısa bir süre önce, egzamada biyofilmlerin (yüzeylere yapışan ve bağışıklık saldırılarına da, antikorlara da çok dirençli olan bakteri kolonilerinin) payı olabileceğine ilişkin yeni bir olasılık öne sürdü. Biyofilmler cilt kanallarını tıkadığı ve içsel bağışıklık yanıtlarını tetiklediği için inatçı cilt sorunlarına yol açabileceğini söyledi. Allen, Laym spiroketlerinin biyofilm oluşturduklarını gösteren çalışmalardan haberdardı. Bu da onun, biyofilmlerin Alzheimer hastalığında da rol oynayıp oynamadığını merak etmesine neden oldu. Ölen Alzheimer hastalarının beyinlerindeki biyofilmlerin konumlarına bakan Allen, amiloid plakları ile aynı hippokampal yerlerde olduklarını gördü. Toll-benzeri almaç 2 (TLR2) adı verilen önemli içsel bağışıklık elemanının da, Alzheimer'lı beyinlerin aynı bölgesinde bulunduğu, fakat kontrol grubu beyinlerde olmadığı saptandı. Allen, TLR2'nin bakterilerin varlığı dolayısıyla etkinleştiğini, fakat biyofilmler nedeniyle içeride sıkıştığından, çevresindeki dokuya zarar verdiği varsayımını ileri sürdü.
 Alzheimer'lı insan beyninin hippokampal bölümündeki biyofilmler ve amiloid-β görülüyor. (COURTESY OF HERBERT ALLEN)
Alzheimer'lı insan beyninin hippokampal bölümündeki biyofilmler ve amiloid-β görülüyor. (COURTESY OF HERBERT ALLEN)Ağız mikrobiyomunun alışıldık bir üyesi olan spiroketler, kan dolaşımında olduklarında (örneğin aktif Laym enfeksiyonlarında veya ağız ameliyatından sonra) kan-beyin engelini aşabilen az sayıdaki mikroptan biridir. Ancak, bu bakteriler o kadar yavaş bölünür ki, bir biyofilm oluşturmaları onlarca yıl alabilir. Bu durumun, Alzeimer hastalığının bir yaşlılık hastalığı olmasıyla örtüştüğünü düşünen Allen, sifilis vakalarının da (spiroketlerin nöroinvazif etkileri, birincil enfeksiyondan 50 yıl kadar sonra ortaya çıkabiliyor) bunu kuvvetlendirdiğini belirtiyor.
Allen'ın çalışması, Alzheimer hastalığının gelişimi ile ilgili uzun süredir bir köşeye atılmış hâldeki bir hipotezi diriltti. 30 yıldan bu yana, patojenik mikropların, hastalığın nöropatolojisini tetikleyebileceği olasılığını araştıran bir avuç bilimci var. Bu kişilerin çoğu, söz konusu bağlantıya şans eseri rastlamış; tıpkı Allen gibi. Onca eleştiriye ve tüm o kaynak bulma ve yayın yapma sorunlarına rağmen, bazıları hayatını bu konuya adamış. Miklossy, zaman içinde çok sayıda gözlem birikmesine rağmen, kendisine aptal gözüyle bakıldığını ve kaynak sağlanmadığını anlatıyor. Yine de spirochetes'in Alzheimer hastalığında payının olup olmadığını araştırmaktan vazgeçmemiş. "Ben Hipokrat Yemini etmiş bir doktorum. Elimizden ne geliyorsa yapmamız gerek," diyor.
Şimdilerde Alzheimer alanında çalışan bilimciler, hastalığın doğuşunu açıklayabilecek bir kuram peşinde. Bilimciler hâlâ hastalığın hangi özelliklerinin, hastalığın ilerleyişi ile ilgili olduğunu kesin olarak söyleyemiyor: Nöroenflamasyon mu, tau düğümleri mi, amiloid plakları mı? Bu netleştirilmediği için de tedavi için işe yarar hedefler belirlenemiyor. Şu ana dek, klinik teste sokulan ilaçların çoğu amiloid-beta peptitini (Alzheimer'lı beyinlerin karakteristiği olan amiloid plaklarının ana bileşenini) hedef alan ilaçlar oldu. Amiloid-beta birikiminin nöropatolojiye yol açtığı ve dolayısıyla amiloid-betanın olmamasının (üretimi azaltılarak, yayılımı azaltılarak veya molekülün beyinden atılmasına yardım edilerek) demans belirtilerini azaltabileceği ya da en azından artmasını engelleyebileceği düşünüldü. Fakat şimdilik araştırmacıların eli boş kaldı.
Örneğin Kasım 2016'da, Eli Lilly'nin (ABD merkezli bir ilaç firması) amiloid hedefli antibiyotiği "solanezumab"ın Faz 3 denemesi, erken evredeki hastalarda iyileşme sağlamadı. Bu pahalıya mal olan ve yıkıcı bir başarısızlıktı. Birkaç ay sonra olayın bir benzeri daha gerçekleşti. Merck (bir başka ABD merkezli ilaç firması), amiloid-beta üreten enzimi bloke eden "verubecestat" adlı küçük-molekül ilacının klinik denemelerini sonlandırdı.
Bunlar, Alzheimer için geliştirilen ve klinik denemelerde hiçbir yararı görülemeyen deneysel ilaçlar zincirine eklenen son iki üyeydi. Denemeleri suçlayanlar da var. Moleküler nörolog John Hardy, klinik denemelerde kalitenin düşük olduğunu söylüyor. Azıcık ilacın daha beyne varış bile yapamadığını vurguluyor. Bazı araştırmacılar ise ilaçların temelindeki kuramı sorguluyor. Etkin ilaçların geliştirilmesinde süregiden başarısızlıkların ışığında, hastalığa ilişkin alternatif kuramların üretilmesi için çaba gösterilmesi gerektiğini düşünenler var. "Bence Alzheimer hastalığı ile ilgili hipotezlerin, amiloid plakları, düğümler ve inflamasyonun yanı sıra, enfeksiyonu da içermesi gerek," diyor Harvard nörobiyologlarından Rudolph Tanzi.
 Bakteriyal veya viral enfeksiyonlar ile Alzheimer hastalığının nöropatolojisi arasındaki bağlantıya ilişkin kanıtlar artıyor. © KIMBERLY BATTISTA
Bakteriyal veya viral enfeksiyonlar ile Alzheimer hastalığının nöropatolojisi arasındaki bağlantıya ilişkin kanıtlar artıyor. © KIMBERLY BATTISTAMikrobiyal Bağlantıların Tarihçesi
Herpes simplex virüsü tip 1 (HSV1), beyni şiddetli şekilde enfekte edebilir ve ender görülen çok ciddi bir beyin iltihabına yol açabilir. 1980’lerin sonlarında, Manchester Üniversitesi’nden moleküler virolog Ruth Itzhaki, HSV1 hastalarında etkilenmiş beyin bölgelerinin, Alzheimer hastalarında hasar almış beyin bölgelerinin aynısı olduğunu fark etti. Herpes'in vücutta uzun süreler boyunca belirti vermeden saklanabileceğini bildiğinden, enfeksiyon ile nörodejeneratif bozukluk arasında nedensel bir bağlantı olabileceği Itzhaki'nin aklına geldi.
Alzheimer hastalarının beyinlerinde HSV1 DNA'sı aramaya başlayan Itzhaki, aradığını buldu. Fakat bu viral DNA, aynı yaşlardaki kontrol grubu beyinlerde de mevcuttu. O zamanlar yeni bir teknik olan PCR (polimeraz zincir tepkimesi) kullanmak zorluklarla doluydu ve Itzhaki'nin bulgularına kontaminasyon (bulaşma/kirlenme/safsızlık) kaynaklı denilerek meydan okunuyordu. Itzhaki çalışmasını büyük bir titizlikle yineledi. İleri yaştaki insanların, Alzheimer olsunlar ya da olmasınlar, üçte ikisi ilâ dörtte üçünün beyinlerinde HSV1 olduğunu yine buldu.
Ardından, neden HSV1 bulaşmış bireylerin sadece bir kısmında demans geliştiğini açıklamak için genetik farklılıkları incelemeye başladı. Sonunda 1997 yılında, beyinde hem HSV1 hem de apolipoprotein E gen varyantı APOE4 taşıyor olmanın, ele aldığı Alzheimer vakalarının %60'ını açıklayabildiğini rapor etti; her iki etkenin tek başına yapabildiğinden çok daha yüksek bir orandı bu. Ama Alzheimer araştırmacılarının çoğu, Itzhaki'nin çalışmasını yine gözardı etti. Onların kendi düzenlerini kurmuş olduklarını ve plaklar ile düğümleri içeren senaryolara fazlasıyla bağlandıklarını belirtiyor Itzhaki. "Virüsler hakkında bilgileri yok; özellikle de herpes virüsünün bedende ve beyinde saklı kalabileceğinden. Virüsün bir şeye neden olabileceği söylendiği anda, senaryonun çok hızlı gelişeceğini düşünüyorlar. Bu çok safça bir düşünce," diyor.
Aynı sıralarda, o dönem İsviçre'deki Lozan Üniversitesi'nde olan nöropatolog Miklossy, hem nörosifilis, hem de Laym bakterilerinin neden olduğu bir sendrom olan nöroborelya için spiroket kaynaklı beyin hasarını detaylandırıyordu. Bakteriyal işgal ve plak oluşumu kanıtı sunan bir kafa travması vakasına denk geldi ve dikkatini Alzheimer'a yöneltti. 14 tane Alzheimer hastasının beyin dokularından spiroket yalıtırken, 13 tane aynı yaştaki kontrol grubu beyinlerde hiç spirokete rastlamadı. Buna ek olarak, amiloid öncü proteinini (APP, yani amiloid öncü proteini bölündüğünde amiloid-beta oluşturur) hedef alan monoklonal antikorların , bulunan spiroket türleri ile çapraz tepkimeye giriyordu; ki bu da bakterilerin, proteinin kaynağı olduğuna işaret ediyordu. 1993'te yayımladığı bulgularına biraz olumlu tepkiler alabilmesine rağmen, Miklossy de tıpkı Itzhaki gibi kuşkuculuktan payına düşeni aldı. Çalışmasına yapılan eleştirilerde "aptalca, doğru bilinene aykırı ve çılgınlık," gibi yorumlar da olduğunu anlatıyor.
Bu arada ABD'de, Alzheimer ile mikrobiyal enfeksiyon arasında bağlantı olabileceğine ilişkin üçüncü bir kanıt dalgası oluşmaya başlamıştı. MCP Hahnemann Tıp Okulu mikrobiyologlarından Alan Hudson, bir dolandırıcılık araştırma komitesinde görev yaparken Brian Balin ile tanıştı. Çok geçmeden nöropatolog Balin, Hudson'a Alzheimer'lı beyin dokuları göndermeye ve hücre içinde Chlamydia cinsinden bakterilerin olup olmadığını sınamasını istemeye başladı. Bazı örneklerde C. pneumoniae için test pozitif çıktı. Bakteriler, Alzheimer nöropatolojisi ile ilişkilendirilen beyin bölgelerindeki (hippokampus ve diğer limbik sistem alanlarındaki) mikroglia ve astrositlerde bulunuyordu. Hudson, sonuçları Balin'e bildirmeden önce testleri bir başka teknisyene daha tekrarlattı. Negatif çıkanların hepsi kontrol grubu beyinler iken, pozitif çıkanların hepsi Alzheimer'lı beyinlerdi. "Ağzımız açık kaldı," diyor Hudson. Bulgularını duyurdukları makaleyi yayımladıklarında, Balin, Hudson ve çalışma arkadaşları dünya basınında yer buldu. Ama Alzheimer araştırmacıları toplantısına katıldıklarında, kendileri ile kimsenin muhattap olmadığını söylüyor Hudson.
Böylece 1990'larda, farklı organizmaları inceleyen ve farklı ülkelerde bulunan üç laboratuvar, Alzheimer hastalığının nedenleri arasında insan patojenlerinin olabileceğine ilişkin işaretlere sahip olmuş oldu. Kuramcılar için ise Alzheimer hastalığının mikrobiyal enfeksiyon bileşeni olabileceği düşüncesi hâlâ kabul edilemezdi.
 Transjenik fareler (en üst sıra), beyinlerine Salmonella girdikten 48 saat sonra, ilgili bölgelerde yüksek düzeyde amiloid-beta oluşturdular. (REPRINTED WITH PERMISSION FROM D.K.V. KUMAR ET AL., SCI TRANSL MED, 8:340RA72, 2016.)
Transjenik fareler (en üst sıra), beyinlerine Salmonella girdikten 48 saat sonra, ilgili bölgelerde yüksek düzeyde amiloid-beta oluşturdular. (REPRINTED WITH PERMISSION FROM D.K.V. KUMAR ET AL., SCI TRANSL MED, 8:340RA72, 2016.)Yeni Yüzyıl, Yeni Mekanizmalar
2016 yılında Itzhaki, Miklossy, Hudson, Balin ve 29 başka bilimci daha, mikropların Alzheimer hastalığının oluşumundaki katkısına işaret eden kanıtları derledikleri bir makaleyi, Journal of Alzheimer’s Disease dergisinde yayımladı. Makalenin başında şöyle bir çağrı vardı: "Bizler, Alzheimer hastalığı üzerinde çalışan araştırmacılar ve klinisyenleriz . . . ve hastalığın bir yönünün görmezden gelinmesi konusundaki kaygımızı ifade etmek için yazıyoruz."
Derginin editörü olan ve Texas Üniversitesi'nde araştırmalarını sürdüren George Perry, makalenin basılmasını kabul etmenin yanı sıra, yazar olarak da imzasını atmış. "The Journal of Alzheimer’s Disease dergisi, her türlü farklı düşünceye açık. Biz popülariteyi önemsemiyoruz," diyor Perry.
Yavaş ve emin adımlarla, Alzheimer araştırmacıları sonunda patojen hipotezini derinlemesine incelemeye karar vermiş gibi görünüyor. En yeni mikrobiyal kuramcılardan Tanzi, Alzheimer alanında onlarca yıldır öne çıkan bir isim. 1987 yılındaki APP geni keşfine (keşfedilen ilk Alzheimer bağlantılı gen) katkıda bulunmuştu. Yakın zamanda, Tanzi ve çalışma arkadaşları, amiloid-beta'nın deney tüpünde patojenik bakterilerin (Candida albicans, E. coli ve Staphylococcus aureus dahil) çoğalmasını engellediğini gösterdi. Bu da, Alzheimer ile ilişkilendirilen bu peptitin, antimikrobiyal görevi gördüğüne işaret ediyor.
Tanzi'nin işleyiş hipotezi şöyle: Mikroplar, içsel bağışıklık tepkisi tetikliyor ve amiloid-beta bunda kilit rol oynuyor. Peptit, sağlıklı dokuyu işgalcilerden korumak için enfeksiyon bölgesine duvar örüyor. Fakat çok miktarda yığılma olduğunda da, bundan dolayı (örülen koruyucu duvarlardan dolayı) sorunlar çıkmaya başlıyor. Plaklar, nöron ölümlerine yol açmaya başlıyor.
Tanzi'nin ekibi tarafından yapılan bir diğer çalışmada, amiloid-beta'nın mikroplara tutunduğu ve diğer amiloid-beta'lara bağlanarak, işgacileri kapana kıstırdığı, böylece onların konak hücre ile etkileşmelerini engellediği ortaya kondu. Kuşkusuz, Alzheimer hastalığının transjenik bir fare modelinde, Salmonella enfeksiyonu beyindeki amiloid plaklarının temelini atmıştı. "Plaklar, hippokampus ve temporal kortekste üretilmişti; buralar, kan-beyin bariyerinin aşılmasına en açık bölgelerdir," diyor Tanzi. Buraların, patojenlerin girmeyi başardığı ilk yerler olduğuna işaret ediyor.
Tanzi, Miklossy'nin ve diğerlerinin aldıkları eleştirilerin farkındaydı. Kendi alacağı eleştirileri de bekler vaziyette şunları söylüyordu: "Her şeyi doğru yapmaya çalıştık, tüm kontrolleri yaptık. Bu makale üzerinde sekiz yıl çalıştık." Fakat onu şaşırtan bir şekilde, çok fazla olumsuz tepki gelmedi. Alzheimer araştırmacılarının sonunda mikrop kuramı üzerinde düşünmeye başladıklarının bir göstergesi olsa gerekti bu.
 Alzheimer nörodejenerasyon patolojisi ile enfeksiyon arasındaki bağlantıyı açıklamaya çalışan çeşitli hipotezler bulunuyor. © KIMBERLY BATTISTA
Alzheimer nörodejenerasyon patolojisi ile enfeksiyon arasındaki bağlantıyı açıklamaya çalışan çeşitli hipotezler bulunuyor. © KIMBERLY BATTISTAAma yine de bu düşüncenin taraftarları kuşkuyla karşılanıyor. New Mexico Sağlık Bilimleri Merkezi'nden moleküler nörobiyolog Elaine Bearer, HSV1 ile Alzheimer nöropatolojisini bağlantılandıran çalışmasını sunduğunda karışık tepkiler almış. Bearer'in temel araştırma konusu, moleküler motorların dev kalamar aksonda kargoyu nasıl teslim aldıkları ve deneysel kargo olarak da HSV1 kullanıyor. Çünkü HSV1'in aksonal ulaştırma rotaları boyunca her iki yönde de seyahat ettiği biliniyor. Enfeksiyon sırasında, HSV1 duyusal sinir uçlarından sinir hücresinin kendisine gidiyor ve burada saklanabiliyor. Etkinleştiğinde, HSV1 tekrar sinapslara dönüyor, epitelyal hücreleri yeniden enfekte ediyor ve işte: Yine bir uçuk!
Bearer 2006 yılında, HSV1'in aksonal ulaştırma mekanizmasına tutunmak için APP kullandığını buldu. Bunun sonucunda, HSV1 APP'yi nöron içine yeniden dağıtıyordu. Yani APP, enfekte olmamış hücrelerde gerçekleşmeyen yollarla birikebiliyordu. Kısa bir süre önce de virüsün APP'ye "bir şeyler yaptığı" anlaşıldı. "Epitelyal hücrelerde, proteinde 25 kat artışa neden oluyor," diyor Bearer. Bu da, proteinin sentezinin enfeksiyona da yanıt verdiğini akla getiriyor.
Bearer ayrıca HSV1'in insan beynindeki amiloid plaklarında kıstırıldığına ilişkin kanıtlar da ortaya koydu. Bu çalışmasının sunumunu yaptı, fakat Eylül 2017 itibariyle henüz yayımlanmış değil. Elde ettiği bulgular, Tanzi'nin bir hayvan modeldeki amiloid plaklarının içinde bulduğu Salmonella bulgusu ve Allen'ın insan beyin dokusundaki amiloid-beta ile aynı yerdeki bakteriyal biyofilm bulgusu ile uyuşuyor.
Alzheimer hastalığını mikrobiyal kuramını destekleyen kanıtlar artmasına rağmen, bu yöndeki çalışmalar için finansman bulmak hâlâ kolay değil. Yaklaşımı eleştiren bilimci sayısı da hâlâ çok fazla. Örneğin mikrobiyal kurama ikna olmadığını belirten Hardy'nin itirazları şunlar: Birincisi, mikropların Alzheimer nöropatolojisine neden olması fikri, hastalığın kalıtımsal yönünü açıklamıyor. Ayrıca plakların ve düğümlerin hasta beyinlerdeki karakteristik anatomik dağılımını da açıklamıyor. Hardy, kan kaynaklı hastalıkta, dağılımın beyinde daha yaygınlaşmış durumda olması gerektiğini düşünüyor. Durumun epidemiyolojiye, nöropatolojiye ve genetiğe uygun düşmediğini söylüyor. Düşüncesini değiştirmesi için daha fazla deneysel kanıt talep ediyor. Neden-sonuç ilişkisini açıkça gösteren deneyler yapılmasını istiyor: Fareyi enfekte edin ve hastalığı gösterin, diyor.
Mikrop kuramcıları, önerdikleri mikrobik tetiklemenin, Alzheimer'ın tek nedeni olmadığını söylemekten çekinmiyor. Itzhaki'nin çalışmasında, vakaların %40'ı HSV1 enfeksiyonu ile açıklanmıyordu. Elbette Alzheimer'ın enfeksiyon ile bağlantılı olması fikri, belli tek bir patojen ile sınırlı değil. Hipotez şundan ibaret: Enfeksiyonun ardından, bazı patojenler beyne sızıyor. Burada tetiklenen bağışıklık tepkisi sonucunda, amiloid-beta birikimi başlıyor ve plak oluşumu gerçekleşiyor.
Alzheimer hastalığına ilişkin, şu anda elimizde yanıttan çok, soru var. Başarısızlığa uğrayan çok sayıda ilaç var ve Alzheimer'a neden olan etkenler net olarak belirlenemiyor. Bilimcilerin inceleyebildiği örneklerde, hastalık hep çok ilerlemiş oluyor. Beynin sonuçta ne hâle geldiğine bakıp, onu o duruma getiren süreci tahmin etmek ise kolay olmuyor. Bilinen bir şey var ki, amiloid bu hastalıkta önemli. Ama hastalığın merkezinde olan ile hastalığın nedeni olan şeyler her zaman aynı olmuyor. Dünyanın her yanından binlerce araştırmacı tarafından gece-gündüz üzerinde çalışılan bu hastalığa bir an önce çare bulunmasını umuyoruz.
Kaynak ve İleri Okuma
- The Scientist, "Do Microbes Trigger Alzheimer’s Disease?" ";
Etiket
Projelerimizde bize destek olmak ister misiniz?
Dilediğiniz miktarda aylık veya tek seferlik bağış yapabilirsiniz.
Destek Ol
Yorum Yap (0)
Bunlar da İlginizi Çekebilir
09 Nisan 2016
Öldürücü Göç : Metastaz
23 Mart 2015
Umut Verici Yeni Alzheimer Tedavisi