Kimyasal Tepkimenin Gerçekleşme Anı Gözlemlendi
Kimyanın, genellikle içerisinde bilinmezlikleri en çok barındıran bilimlerden biri olduğu düşünülür. Birkaç kimyasalı birbiriyle karıştırırsınız ve bir anda tamamen farklı bir m...
Kimyanın, genellikle içerisinde bilinmezlikleri en çok barındıran bilimlerden biri olduğu düşünülür. Birkaç kimyasalı birbiriyle karıştırırsınız ve bir anda tamamen farklı bir madde elde edersiniz. Bu gizemli havadan olacak ki, reaksiyona giren maddelerin tam olarak hangi anda ürünlere dönüştüğünün gözlemlenmesinin imkansız olduğu görüşü de oldukça yaygındır.
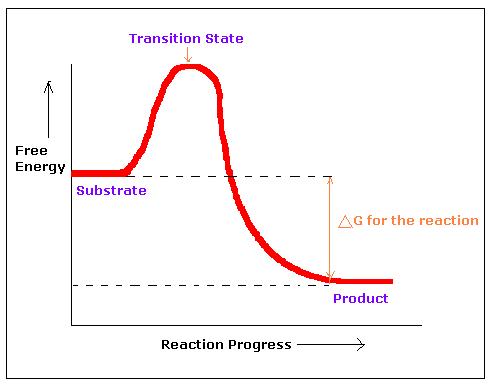 Fakat, bilim insanları, reaksiyon gerçekleşirken ilk defa bu anlık formları, yani reaksiyona giren maddelerin tam olarak ürünlere dönüştüğü anı gözlemlemeyi başardılar. Massachusetts Institute of Technology’den (MIT) bilim insanları, kimyasal reaksiyonların karmaşıklığından dolayı daha önceleri reaksiyon sırasında ölçülmesinin imkansız olduğu düşünülen geçiş evresinin (transition state) enerjisini ölçtüler.
Fakat, bilim insanları, reaksiyon gerçekleşirken ilk defa bu anlık formları, yani reaksiyona giren maddelerin tam olarak ürünlere dönüştüğü anı gözlemlemeyi başardılar. Massachusetts Institute of Technology’den (MIT) bilim insanları, kimyasal reaksiyonların karmaşıklığından dolayı daha önceleri reaksiyon sırasında ölçülmesinin imkansız olduğu düşünülen geçiş evresinin (transition state) enerjisini ölçtüler.
Geçiş evresi, tepkiyenler ve ürünlerin arasındaki kimyasal reaksiyonun ilk evresidir. Josh Baraban’ın belirttiğine göre; tepkiyenler ve ürünler bir dağın iki tarafındaki ovalarda bulunurlar. Reaksiyonu gerçekleştirmek için bu aradaki dağı aşmaları gerekir. Reaksiyonlar üzerine yapılan hesaplarda, genellikle bir dağ olarak tanımladığımız geçiş evresi doğrudan çalışabilecek bir şey olarak görülmez.
Araştırma takımı yaptıkları çalışmada, izomerizasyon olarak adlandırılan kimyasal süreci çalıştılar. Bu süreçte bir molekül, aynı atomlara sahip fakat farklı dizilişteki başka bir moleküle dönüşür. Araştırmacıların spesifik olarak üzerinde çalıştıkları molekül de, birbirine 3’lü bağ ile bağlanmış 2 karbon atomu ve bu karbon atomlarına da bağlı birer hidrojeni olan, asetilen.
Bulguları Science dergisinde yayımlanan çalışmada araştırmacılar, asetilenin U şeklindeki molekül düzeninden ( hidrojenler karbon atomlarının üst kısmında bulunuyor) zigzag molekül şekline (hidrojenlerden birisi yukarı diğeri aşağıya bakacak şekilde karbon atomlarına bağlılar) dönüşme reaksiyonunu gözlemlediler. Moleküllerin içerisindeki atomlar titreşim halinde olduklarından dolayı eğer moleküle daha fazla enerji verilirse, titreşimlerin hızı artıyor. Araştırmacılar, asetilen molekülünün titreşim durumunu ölçtüler ve daha yüksek enerji sağladıklarında düzenli bir görüntü olduğunu farkettiler. Tahmin edilen bu düzen, daha sonra molekül belirli bir enerji seviyesine geldiğinde aniden bozuldu. Bu enerji seviyesi aşıldıktan sonra da, molekülde oldukça düşük frekanslarda titreşimsel enerji gözlemlendi. İzomerleşme meydana gelmişti.
Baraban’ın belirttiğine göre, araştırmacılar, bozulan düzenin spesifik olarak iki biçim arasındaki geçiş evresinde meydana gelmiş olması gereken belirli yapısal değişikliklerle ilişkili titreşimleri içerdiğini gördüler.
Araştırmacılar basit bir şekilde bu durumu yalnızca gözlemlemekle de yetinmediler. Ayrıca, geçiş evresinin enerjisinin hesaplanabilmesini sağlayan ve kimyacıların reaksiyon hızını çalışmasına yardımcı olacak bir de formül geliştirdiler. Fakat, bu formül şu anda yalnızca izomerleşme üzerinde denenmiş durumda olmasına rağmen, araştırmacılar diğer kimyasal reaksiyonlara da uygulanabilir olduğunu düşünüyorlar.
Kaynak: ''Spectroscopic characterization of isomerization transition states'' Science 11 December 2015: Vol. 350 no. 6266 pp. 1338-1342 DOI: 10.1126/science.aac9668
 Fakat, bilim insanları, reaksiyon gerçekleşirken ilk defa bu anlık formları, yani reaksiyona giren maddelerin tam olarak ürünlere dönüştüğü anı gözlemlemeyi başardılar. Massachusetts Institute of Technology’den (MIT) bilim insanları, kimyasal reaksiyonların karmaşıklığından dolayı daha önceleri reaksiyon sırasında ölçülmesinin imkansız olduğu düşünülen geçiş evresinin (transition state) enerjisini ölçtüler.
Fakat, bilim insanları, reaksiyon gerçekleşirken ilk defa bu anlık formları, yani reaksiyona giren maddelerin tam olarak ürünlere dönüştüğü anı gözlemlemeyi başardılar. Massachusetts Institute of Technology’den (MIT) bilim insanları, kimyasal reaksiyonların karmaşıklığından dolayı daha önceleri reaksiyon sırasında ölçülmesinin imkansız olduğu düşünülen geçiş evresinin (transition state) enerjisini ölçtüler.Geçiş evresi, tepkiyenler ve ürünlerin arasındaki kimyasal reaksiyonun ilk evresidir. Josh Baraban’ın belirttiğine göre; tepkiyenler ve ürünler bir dağın iki tarafındaki ovalarda bulunurlar. Reaksiyonu gerçekleştirmek için bu aradaki dağı aşmaları gerekir. Reaksiyonlar üzerine yapılan hesaplarda, genellikle bir dağ olarak tanımladığımız geçiş evresi doğrudan çalışabilecek bir şey olarak görülmez.
Araştırma takımı yaptıkları çalışmada, izomerizasyon olarak adlandırılan kimyasal süreci çalıştılar. Bu süreçte bir molekül, aynı atomlara sahip fakat farklı dizilişteki başka bir moleküle dönüşür. Araştırmacıların spesifik olarak üzerinde çalıştıkları molekül de, birbirine 3’lü bağ ile bağlanmış 2 karbon atomu ve bu karbon atomlarına da bağlı birer hidrojeni olan, asetilen.
Bulguları Science dergisinde yayımlanan çalışmada araştırmacılar, asetilenin U şeklindeki molekül düzeninden ( hidrojenler karbon atomlarının üst kısmında bulunuyor) zigzag molekül şekline (hidrojenlerden birisi yukarı diğeri aşağıya bakacak şekilde karbon atomlarına bağlılar) dönüşme reaksiyonunu gözlemlediler. Moleküllerin içerisindeki atomlar titreşim halinde olduklarından dolayı eğer moleküle daha fazla enerji verilirse, titreşimlerin hızı artıyor. Araştırmacılar, asetilen molekülünün titreşim durumunu ölçtüler ve daha yüksek enerji sağladıklarında düzenli bir görüntü olduğunu farkettiler. Tahmin edilen bu düzen, daha sonra molekül belirli bir enerji seviyesine geldiğinde aniden bozuldu. Bu enerji seviyesi aşıldıktan sonra da, molekülde oldukça düşük frekanslarda titreşimsel enerji gözlemlendi. İzomerleşme meydana gelmişti.
Baraban’ın belirttiğine göre, araştırmacılar, bozulan düzenin spesifik olarak iki biçim arasındaki geçiş evresinde meydana gelmiş olması gereken belirli yapısal değişikliklerle ilişkili titreşimleri içerdiğini gördüler.
Araştırmacılar basit bir şekilde bu durumu yalnızca gözlemlemekle de yetinmediler. Ayrıca, geçiş evresinin enerjisinin hesaplanabilmesini sağlayan ve kimyacıların reaksiyon hızını çalışmasına yardımcı olacak bir de formül geliştirdiler. Fakat, bu formül şu anda yalnızca izomerleşme üzerinde denenmiş durumda olmasına rağmen, araştırmacılar diğer kimyasal reaksiyonlara da uygulanabilir olduğunu düşünüyorlar.
Kaynak: ''Spectroscopic characterization of isomerization transition states'' Science 11 December 2015: Vol. 350 no. 6266 pp. 1338-1342 DOI: 10.1126/science.aac9668
Kaynak ve İleri Okuma
Etiket
Projelerimizde bize destek olmak ister misiniz?
Dilediğiniz miktarda aylık veya tek seferlik bağış yapabilirsiniz.
Destek Ol
Yorum Yap (0)
Bunlar da İlginizi Çekebilir

19 Haziran 2017
Asal Gazlar Nasıl Işık Verir?
27 Temmuz 2019
Biyokimyasal Benzeri Bir Kimyasal Tepkime Ağı Keşfedildi
06 Temmuz 2017
Suyun İki Farklı Sıvı Formu Olduğu Keşfedildi

15 Nisan 2015
Giysileri Temizlemenin Ardındaki Kimya

20 Şubat 2015
Katı Yakıtlar Yanarken Neden Duman Çıkartırlar?

17 Ocak 2016
Kolaya Çamaşır Suyu Eklenirse Ne Olur?
19 Ekim 2014
Suç Mahali Kimyası – Luminol ve Kan